本文对五元及六元杂芳族磺酰卤——各类化学领域中的关键反应试剂——的稳定性进行了全面研究。基于对200余种该类化合物获得的实验数据,本文确定了数种分解途径,以及各杂环体系的稳定性变化规律。这些途径包括:形式上的二氧化硫(SO₂)脱出(典型发生于吡啶α-与γ-位异构体以及大多数二嗪衍生物)、痕量水引发的水解(典型发生于吡啶β-位异构体及部分唑类化合物)、发生在其他官能团上的反应(底物特异性),以及很可能与杂环自身在亲电基团存在下稳定性有限相关的复杂分解(见于呋喃、异噁唑及部分异噻唑衍生物)。基于这些结果,本文提出用于化学合成中选择合适杂环磺酰卤的简单经验规则,即:选择磺酰氯,还是更稳定但反应活性更低的磺酰氟。
引言
许多化学工作者都遇到过与化合物稳定性相关的问题,而稳定性是试剂与最终产物最重要的性质之一。稳定性问题既影响科研实验室或工业流程中试剂的操作使用,也影响经济层面,包括合成、物流与储存成本。部分研究项目可能因反应性原料或中间体发生分解而在某些步骤中失败。许多化学工作者常将不期望的副反应或低产率归结为“反应本身不好”,却忽略了所使用的试剂可能已经不纯。这些问题在最受关注的化学研究方向中尤为关键,例如紫杉醇全合成,但在药物研发中广泛使用的更简单的化学反应中也同样重要。
在该领域及其他研究领域中,学术界以及更大程度上的工业界倾向使用一套标准的、稳定、可靠且易于获得的起始原料(结构砌块),其反应性可预测。制药及类似行业的交付压力催生了几种主流反应类型,例如酰胺化反应、Suzuki-Miyaura偶联或Buchwald-Hartwig偶联,这些反应因对应反应物的商业化可得性与高选择性而受到青睐。这些反应所需的结构砌块通常可在实验台上稳定存放数年,且供应商通常会提供其稳定性、储存条件与危险警示信息。但对于其他化合物类别,情况并非总是如此,它们有时需要合成、纯化并立即使用而不能储存。
每年都会出现许多新的有机反应乃至对应的结构砌块类型,但通常不会说明其存在的稳定性隐患。熟练的化学家甚至人工智能有时可以预判哪些有机化合物可能存在稳定性–反应性方面的问题。然而在很多情况下,即使是广泛使用的试剂类别,也缺乏相关系统性信息。磺酰氯便是这类试剂的典型例子,它是合成磺酰胺、磺酸酯或砜类化合物的重要结构砌块。众所周知,磺酰氯稳定性有限,有时甚至难以获得。除水解反应性外,它们还可通过烯砜生成或SO₂脱出分解生成相应的氯化物,高温可加速该过程。因此,氯磺化聚乙烯的热分解研究表明,该过程涉及碳–硫键与硫–氯键同时断裂,生成二氧化硫与自由基。
杂芳族磺酰氯的稳定性问题尤为重要。尽管这一事实在经验丰富的合成化学家中众所周知,但在化学文献中却鲜有报道,且该系列化合物的结构–稳定性关系仍未被揭示。1950年,Roblin与Clapp报道苯并噻唑-2-基、4,6-二甲基嘧啶-2-基与1-甲基四氮唑-5-基磺酰氯不稳定,会分解为相应的杂芳基氯。作者提出,许多其他杂芳族磺酰氯应在制备后立即使用以防止分解;此后,这一因素很可能导致了此类化合物商业化可得性受限。异喹啉-1-与-4-磺酰氯分别转化为1-与4-氯异喹啉的过程也在早前被提及。相反,部分化合物如吡啶-2-磺酰氯在文献中记载相对充分,但即使是知名学者在其工作中也未提及它有限的稳定性。
研究者已付出大量努力,用更稳定且仍保持相似反应性的替代物取代磺酰氯。2009年,Bornholdt及其同事报道五氟苯基磺酸酯为可货架稳定的磺酰化试剂,用于制备杂环磺酰胺。2014年,Sharpless及其同事阐述了磺酰氟作为SuFEx(硫氟交换)点击化学反应试剂的通用性与高稳定性。该报道成为磺酰氟应用范围大幅扩展的基础,此后出现大量描述其合成与应用的论文。过去十年间发现,磺酰氟对绝大多数常见合成转化具有耐受性,在合适反应条件下仍可进行磺酰化反应。磺酰氟反应性的另一重要实例为吡啶-2-磺酰氟(PyFluor),一种低成本、稳定且高选择性的脱氧氟化试剂。
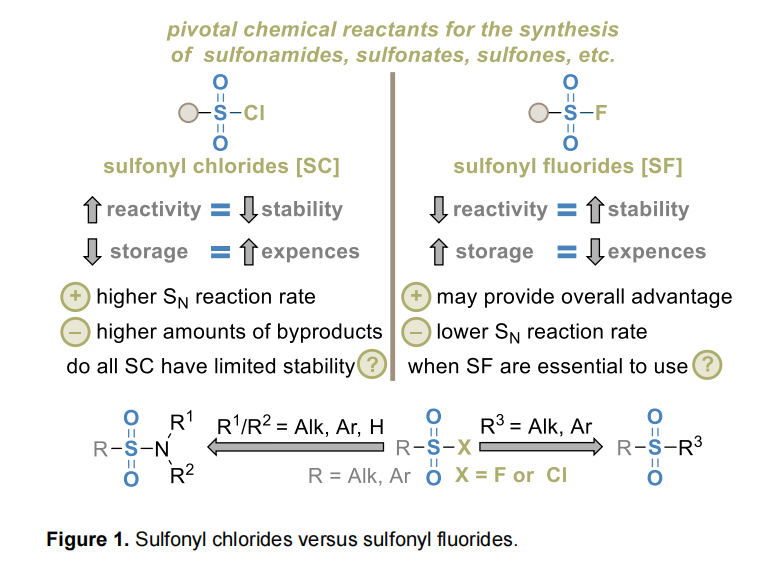
尽管已有上述研究,杂芳族磺酰氯与磺酰氟的系统性稳定性研究仍然缺乏。更重要的是,对于特定杂环取代基,人们仍不清楚是否必须使用磺酰氟,还是反应活性更高的磺酰氯即可适用。仅有少量研究同时考察分子中同时含有磺酰氯与磺酰氟的化合物,结果显示其具有顺序反应性。已有数篇论文研究取代基的立体电子效应对苯磺酰卤系列溶剂解反应速率的影响。
在本工作中,我们旨在对杂芳族磺酰氯与磺酰氟系列的结构–稳定性关系进行全面分析。除芳香杂环在药物发现中的整体重要性以及符合近期“回归平面”理念外,我们关注该类化学结构是因其在电子性质与可获得取代模式上具有高度多样性。大多数例子中存在的碱性氮原子因其对化合物稳定性的直接影响而受到特别关注。此外,我们设想可通过在杂环母核上引入取代基进行空间或电子修饰以提高化合物稳定性。本研究共涉及236个稳定的磺酰卤结构砌块。值得注意的是,其中165个为本文首次专门合成,20个为文献报道但本文首次进行表征。
结果
本文图2所示杂环磺酰卤的合成采用此类化合物的标准方法之一进行,即有机硫(II)衍生物的氧化卤化、直接氯磺化、重氮盐的桑德迈尔型反应,或金属化杂环与SO₂反应,再与亲电卤源反应(更多细节见支持信息中的方案S1–S4及对应文本)。
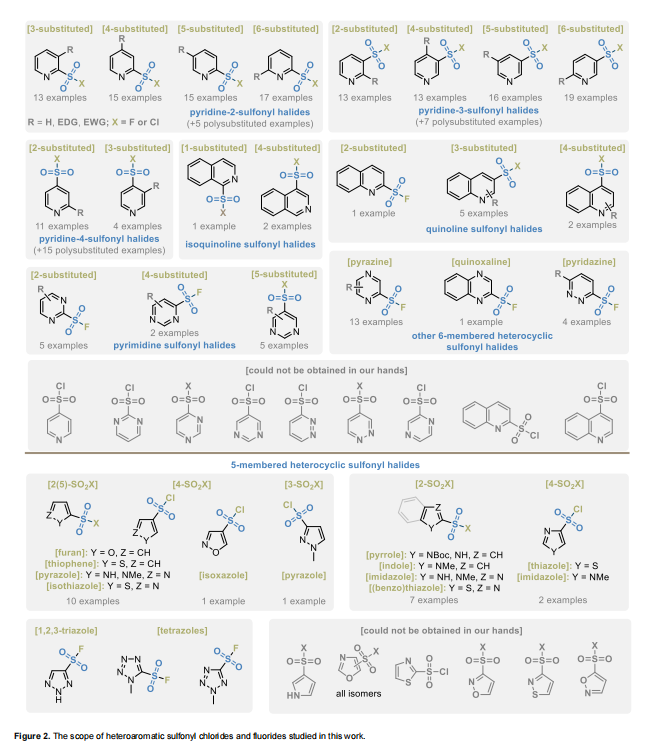
磺酰卤的稳定性通过两组实验进行研究。首先,选取52个模型化合物,包括各系列中相对稳定的母核杂环衍生物,以及部分稳定的单取代吡啶衍生物(用于评估取代基效应)。为每种所选化合物制备两份THF-d₈溶液样品,分别置于NMR管中在+4°C(冰箱中)与室温下储存,在长达14个月的时间内定期测定¹H NMR 谱。我们选择THF-d₈作为溶剂,因其不与磺酰卤反应(如不同于CD₃OD)、吸湿性较低(如不同于 DMSO-d₆)、且不含酸性杂质(如不同于CDCl₃或CD₂Cl₂)。此外,其非氘代类似物(THF)是可用于进行磺酰化反应的溶剂之一。
其次,所有236个纯品磺酰卤在Enamine仓库中于–70°C、–10°C、4°C或室温下储存长达10年,并通过¹H NMR定期检测其质量。正如预期,磺酰卤在溶液中通常更易发生分解,前一组实验受样品性质影响更小,从而给出更清晰的结构–稳定性趋势。对于纯品化合物,其他因素如微量杂质的存在与物理状态可能具有显著影响,因此部分对应趋势可能不够明显。另一方面,可研究的化合物规模大得多。所有化合物的杂芳族磺酰卤稳定性完整实验数据汇总于支持信息表S1与S2。
溶液中的稳定性
在THF-d₈溶液中的稳定性研究结果示于图3与图4(另见支持信息表S1)。在吡啶磺酰氯异构体系列中,观察到如下规律:γ-异构体<α-异构体<β-异构体。因此,母核吡啶-2-磺酰氯在室温下12小时后完全分解,通过SO₂脱出干净生成2-氯吡啶,而吡啶-4-磺酰氯完全无法获得。吡啶-3-磺酰氯在+4°C下稳定超过2个月。室温下,其分解从第1个月开始,半年内原料完全消失。该情况下,水解为主要分解途径,并观察到相应磺酸沉淀。
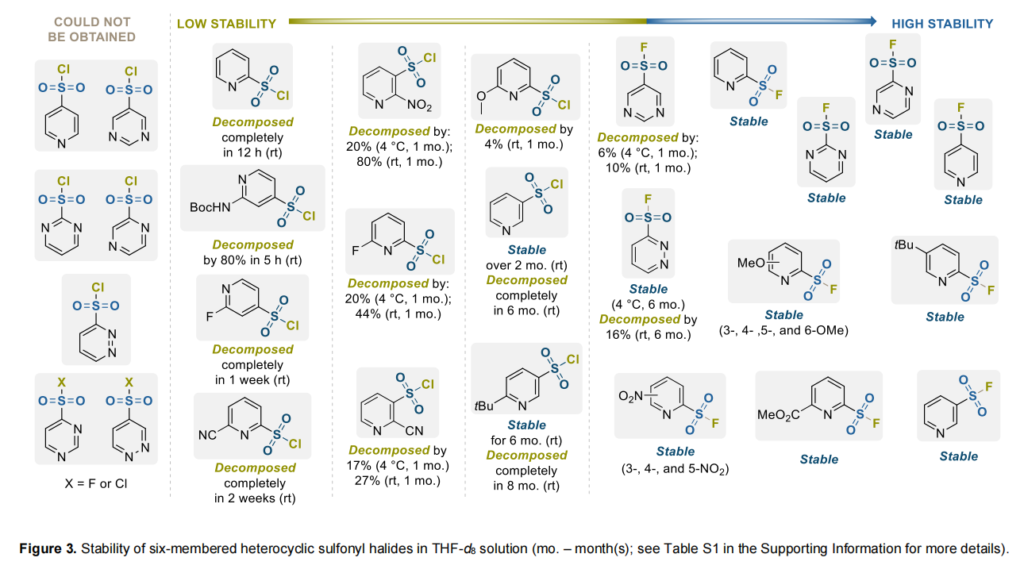
6-位取代的吡啶-2-磺酰氯比对应的母核化合物更稳定。取代基对稳定性的影响遵循如下规律:H<CN<F<OMe<<OtBu。因此,6-叔丁氧基取代的衍生物在室温下稳定至少2个月,而其6-氰基取代的类似物在相同条件下2周内完全分解。所有情况下,SO₂脱出均为主要分解途径,尽管也会出现其他反应(如水解)。
在吡啶-3-磺酰氯的C-2位引入吸电子取代基会显著降低化合物稳定性,这与取代基的电子效应相关。因此,2-硝基衍生物在室温下1个月内分解80%。该情况下,分解产物包括2-氯吡啶-3-磺酰氯与相应磺酸。对应的2-CF₃与2-CN取代物在相同条件下发生显著水解。相反,对吡啶氮原子进行空间屏蔽可在一定程度上提高化合物稳定性:6-叔丁基取代的衍生物在+4°C或室温下稳定半年。其后续分解遵循水解途径。
部分取代吡啶-4-磺酰氯可制备但稳定性有限。2-NHBoc 取代的衍生物在室温下5小时内分解80%,通过SO₂脱出生成相应杂芳基氯。2-氟、2,5-与2,6-二氯吡啶-4-磺酰氯分解速率略低,但在室温下1个月内仍显著降解,主要生成相应SO₂脱出与水解产物——杂芳基氯与磺酸。
相反,所有吡啶磺酰氟异构体,包括带有强共轭给电子基(OMe)或吸电子基(NO₂)的化合物,在THF-d₈溶液中均稳定。
二嗪类磺酰卤的稳定性低于吡啶衍生物。因此,所有对应的母核磺酰氯以及嘧啶-与哒嗪-4-磺酰氟均无法获得。哒嗪-3-磺酰氟在+4°C下稳定6个月,但在室温下缓慢分解,生成哒嗪-3(2H)-酮(很可能通过被水解中断的SO₂脱出)。嘧啶-5-磺酰氟稳定性也有限,室温下1个月内分解10%。基于NMR与GC-MS数据,我们认为发生了水合反应;此类反应性常见于C-5位带有吸电子取代基的嘧啶。相反,吡嗪-2-磺酰氟与嘧啶-2-磺酰氟保持稳定。
五元杂芳族磺酰卤通常稳定性低于其六元环类似物。因此,所有四种呋喃与噻吩衍生的磺酰氯在THF-d₈溶液中于4°C或室温下缓慢分解。3-位取代衍生物的稳定性低于其2-位异构体,而杂环类型影响很小。对于噻吩衍生磺酰氯,主要分解产物为相应磺酸;而对于呋喃,生成复杂的未知产物混合物。
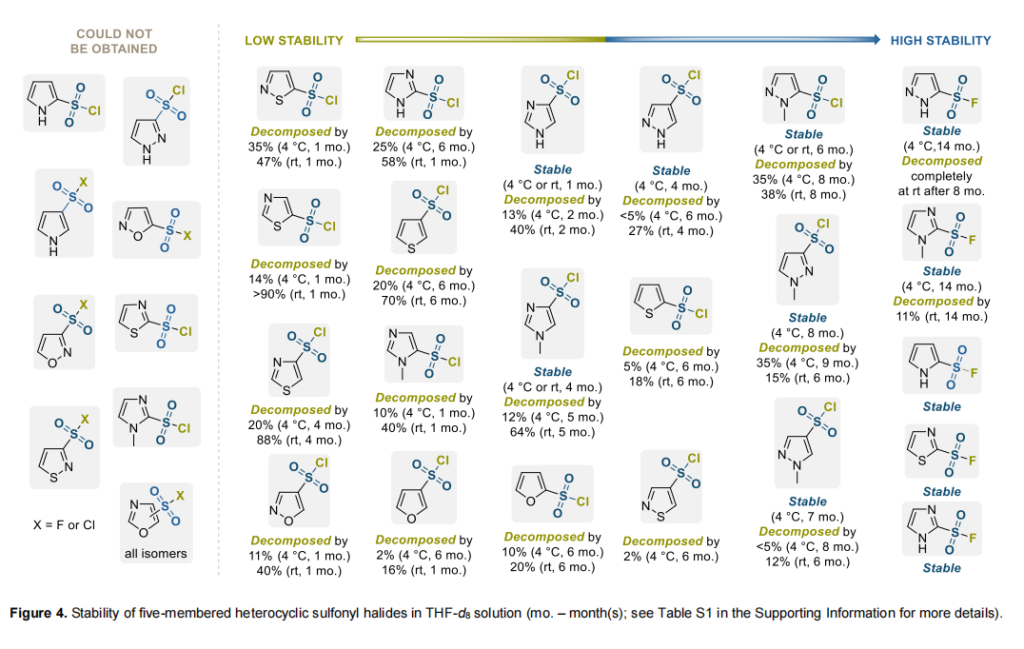
值得注意的是,所有吡咯-3-磺酰卤(氯或氟)均无法获得。对于吡咯-2-磺酰卤,对应的氯因过于不稳定而未合成,而氟则易于处理,在溶液中14个月内无变化。
本文研究的母核异噁唑与异噻唑衍生磺酰卤在THF-d₈溶液中稳定性也有限。异噁唑-4-磺酰氯在1个月后于4°C与室温下分别分解11%与40%。异噻唑-4-磺酰氯更稳定,在4°C下约半年后才出现部分分解。其5-位异构体稳定性低得多,1个月后于4°C与室温下分别分解35%与47%。所有情况下均生成复杂的未知产物混合物,很可能因杂环发生破坏。
异噁唑-3-、异噻唑-3-与异噁唑-5-磺酰卤均无法获得。我们认为,后一种情况的结果可能与化合物本身稳定性无关,而是异噁唑环在磺酰卤合成条件下稳定性有限(文献已报道少量芳基取代衍生物)。噻唑系列出现类似情况。噻唑-4-与-5-磺酰氯均在1个月后开始分解,且5-位更快。噻唑-2-磺酰氯完全无法获得,而对应的磺酰氟在14个月内保持不变。
母核噁唑衍生磺酰卤均无法获得。同样,至少部分化合物的结果可能与化合物本身稳定性无关,而是噁唑在磺酰卤合成条件下难以官能化。
总体而言,吡唑与咪唑衍生磺酰卤在所研究的唑类衍生物中最为稳定。因此,所有三种1-甲基吡唑磺酰氯异构体在THF-d₈溶液中于4°C下稳定超过半年。此后观察到水解,并伴随相应磺酸沉淀。室温下得到类似结果。
母核吡唑-4-磺酰氯表现出相似稳定性;其分解遵循水解途径。我们无法合成吡唑-3(5)-磺酰氯,但对应的磺酰氟在4°C或室温下14个月内均稳定。
1-甲基咪唑-4-磺酰氯在4°C或室温下稳定超过4个月;此后部分水解为相应磺酸。其5-位异构体水解快得多:1个月后,4°C与室温下分别剩余90%与60%原料。1-甲基咪唑-2-磺酰氯无法以纯品获得。对应的磺酰氟在4°C下14个月内稳定,但在室温下缓慢水解生成相应磺酸。
两种母核咪唑磺酰氯稳定性均有限。因此,咪唑-2-磺酰氯在4°C下分解25%,生成2-氯咪唑、咪唑-1,3-二氢-2H-咪唑-2-酮与相应磺酸的混合物。室温下,1个月后仅剩余约40%原料。该情况下,水解为主要分解途径。对应的磺酰氟在THF-d₈溶液中14个月内无变化。咪唑-4(5)-磺酰氯在第1个月内稳定,但此后发生部分水解。
纯品稳定性
以纯品形式储存时,大多数磺酰氯与几乎所有磺酰氟可长时间保持不变(至少2年)。上述THF-d₈溶液中讨论的总体稳定性趋势在纯品中基本成立。但特定取代基效应有时不够明显。分解概率受多种其他因素影响,如样品纯度与物理状态,因此部分电子性质相似的化合物表现不同。此外,即使是同一化合物的不同样品,在某些情况下稳定性也可能不同。
大多数分解现象出现在SO₂Cl位于C-2位的吡啶衍生物中,这既与该类结构稳定性有限有关,也与它们在所研究化合物集中占比较高(25个)有关。如前所述,母核吡啶-2-磺酰氯稳定性有限,制备后一天内分解为2-氯吡啶(通过SO₂脱出)。在C-6位引入给电子取代基(如 Me、OMe、O-tBu或NHBoc)可显著提高化合物稳定性。6-甲基吡啶-2-磺酰氯仍表现出分解趋势(–10°C下不到5个月分解超过50%)。此外,部分6-甲氧基吡啶-2-磺酰氯样品也观察到分解,尽管该化合物通常在–10°C下稳定长达4年。
在吡啶环任意位置引入吸电子基团(NO₂除外)均可使相应磺酰氯的储存稳定性高于母核化合物。卤素、CF₃、CN、COOH、酰胺、酯与N-三氟乙酰氨基等基团均表现出该效应。尽管如此,许多化合物仍观察到分解,如图5所示。显然,杂环C-3或C-5位带有较强吸电子基团(如CO₂Et、F或CF₃)的化合物稳定性更低。相反,5-氯、5-三氟乙酰氨基、5-氟-6-甲基与多个6-位取代吡啶-2-磺酰氯在整个观察期内未出现任何分解产物。4-氟与4-氯吡啶-2-磺酰氯稳定性有限。此外,6-甲基-4-三氟甲基吡啶-2-磺酰氯在–10°C下仅3个月就分解50%。相反,2-氯磺酰基异烟酸在该条件下稳定。
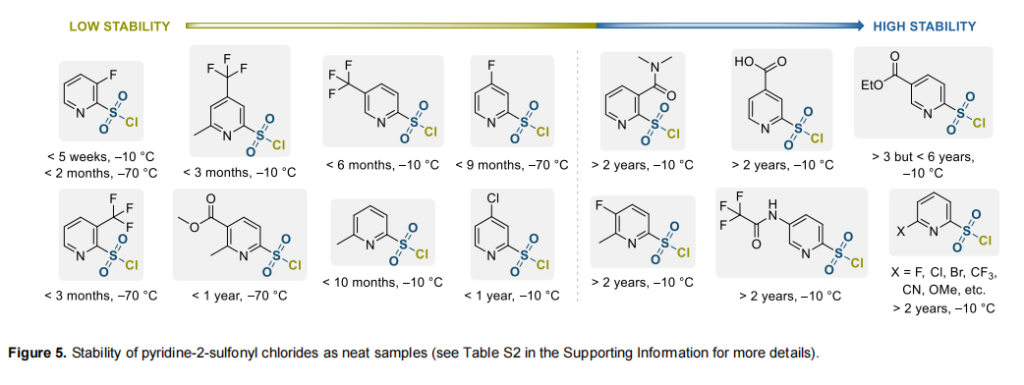
几乎在所有上述情况下,主要分解途径均包括SO₂脱出,生成相应2-氯吡啶衍生物。
如前所述,吡啶-4-磺酰氯在吡啶系列中稳定性最差,因此我们的数据集有限(仅8个化合物)。大多数稳定的化合物在C-6位带有至少一个氟原子,其样品可稳定超过2年。出乎意料的是,6-叔丁氧基吡啶-4-磺酰氯也足够稳定,可在–10°C下储存超过4个月。
吡啶-3-磺酰氯在所研究的杂环磺酰氯中数量最多(45个),若储存得当,几乎所有纯品均可稳定存放数年。发生降解的化合物如图6所示;我们认为这些情况下的分解遵循水解途径。显然,从这些结果中难以总结趋势,很可能因本节第一段所述因素影响。除少数例外,分解需要数年才会发生,且许多其他非常相似的化合物在相同条件下保持稳定。正如预期,降低储存温度可延长样品寿命,部分化合物可证明这一点。另一有趣现象与5-与6-甲基吡啶-3-磺酰氯有关:转化为盐酸盐可显著提高其稳定性。
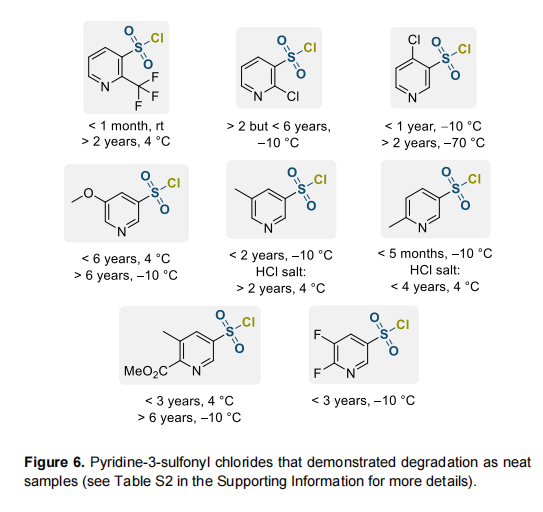
二嗪衍生物中,仅取代嘧啶-5-磺酰氯足够稳定可作为纯品储存。尽管如此,本文研究的五种代表化合物均未观察到降解。
另一值得注意的结果是,在C-2与C-6位引入卤素原子可稳定嘧啶-4-磺酰氯。与THF-d₈溶液中的实验结果相反,五元杂环衍生的15种磺酰氯中有14种在适当纯品储存条件下保持稳定。唯一例外是异噻唑-5-磺酰氯,它在4°C下稳定3年,但在接下来2年内分解30%并生成复杂混合物。正如预期,几乎所有杂环磺酰氟(131个)作为纯品均具有高稳定性,可存放数年。少数例外如图7所示。值得注意的是,磺酰氟的有限稳定性在哒嗪或四氮唑系列中均非普遍趋势。显然,4-氟与4-氯哒嗪-2-磺酰氟的主要分解途径为通过SNAr反应在杂芳基卤位点发生水解。2-甲基-2H-四氮唑-5-磺酰氟的分解产物性质不明确。
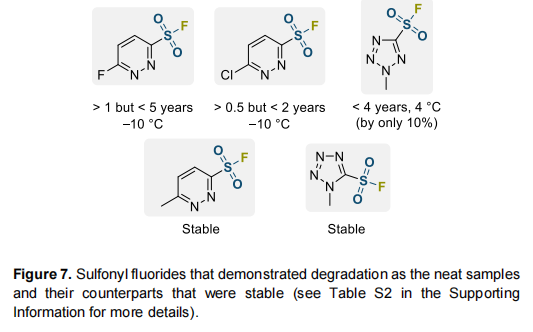
讨论
上述结果表明,磺酰卤(溶液或纯品状态)可通过以下一种或多种反应途径发生分解:
| 1 | 形式上的SO₂脱出,生成相应杂芳基卤(部分情况下被水解中断); |
| 2 | 水解为相应磺酸; |
| 3 | 发生在其他官能团上的反应; |
| 4 | 其他(未确定)分解途径。 |
形式上的SO₂脱出
这是六元杂环α-与γ-位磺酰氯的主要分解途径。上述大量结果证实,当存在提高SO₂Cl基团对芳香亲核取代(SNAr)反应性的因素时,该途径更易发生。如前所述,化合物稳定性遵循如下规律:β-异构体>α-异构体>γ-异构体。此外,在SO₂Cl基团的邻位或对位合理放置吸电子基团会显著加速分解过程。最后,二嗪衍生物稳定性远低于吡啶。
影响六元杂环磺酰氯稳定性的另一重要因素是嗪氮原子的亲核性,这在吡啶系列中清晰可见。实际上,在C-6(2)或C-4位引入吸电子基团可提高α-与γ-异构体的稳定性。空间屏蔽(通过C-6(2)位取代基)也可降低降解速率。这些结果表明嗪氮原子参与分解途径。
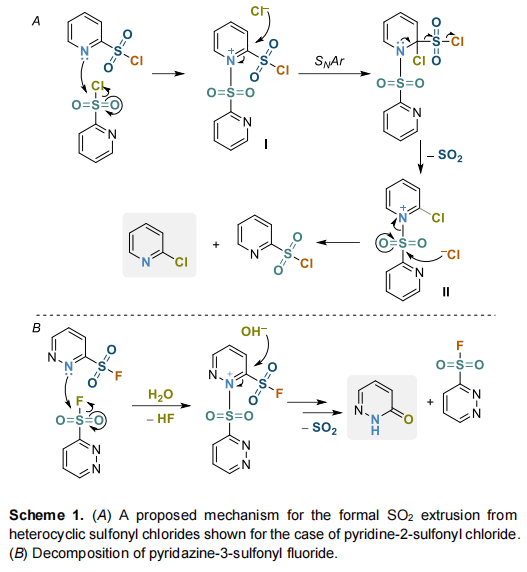
基于这些数据,我们认为反应机理涉及一分子磺酰卤对另一分子的N-磺酰化(方案1,A)。生成的中间体I被氯离子在活化的C-2(或C-4)位进行SNAr进攻,导致SO₂Cl基团被亲核取代,生成2-(或4-)氯吡啶鎓中间体II。脱去SO₂后,剩余氯离子进攻分子II中被活化的磺酰位点,生成预期的氯吡啶衍生物并再生一分子起始磺酰氯。
对于哒嗪-3-磺酰氟,也可能生成I型中间体。但氟离子亲核性不足以进行后续SNAr进攻,因此水分子作为亲核来源,最终生成哒嗪-3(2H)-酮(方案1,B)。咪唑-2-磺酰氯中也检测到类似过程。
水解
该分解途径常见于吡啶-3-磺酰氯以及吡唑、咪唑与噻吩衍生物。由于反应需要痕量水存在,其强烈依赖这一难以控制的因素。吸电子取代基加速该过程,可能与SO₂Cl部分亲电性增强有关。另一方面,给电子基团(如Me)也会提高水解速率。这一结果可通过嗪氮原子参与反应催化进行合理解释(方案2)。值得注意的是,类似的亲核参与也被用于解释磺酰氯的醇解。另一可能反应途径涉及N-磺酰化(与方案1 类似),这会提高SO₂Cl部分对水进攻的亲电性。无论如何,嗪氮原子附近的空间位阻以及转化为盐酸盐形式都会阻碍亲核辅助作用并提高化合物稳定性。
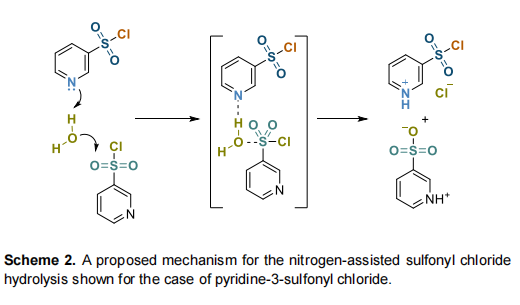
其它官能团上的反应
部分情况下,分解过程因磺酰卤分子中其他官能团的参与而变得复杂。在可能的竞争反应中,SNAr反应相对常见。因此,2-硝基吡啶-3-磺酰氯的水解分解伴随硝基的亲核取代,生成混合产物(方案3,A)。氟化吡啶磺酰氯中也观察到类似过程。
6-氟与6-氯哒嗪-3-磺酰氟的水解以杂环上的SNAr反应进行(方案3,B)。2-氟吡啶-4-磺酰氯与6-氟吡啶-2-磺酰氯中也检测到类似副反应。
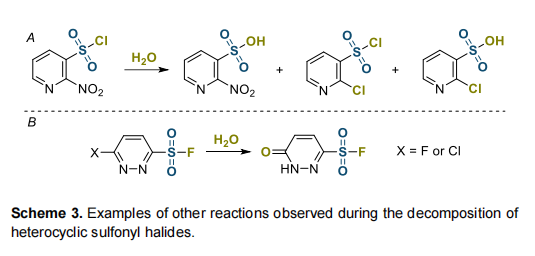
其它分解途径
大量五元杂环磺酰卤分解后生成复杂的未知产物混合物。部分情况下,这可能与杂环体系在强酸(亲电试剂)存在下稳定性有限有关。吡咯、呋喃、异噁唑、噁唑与异噻唑衍生物很可能出现此类行为。噻唑衍生物稳定性有限的原因尚不明确。值得注意的是,尽管在溶液中观察到分解,但大量上述杂环磺酰卤在纯品状态下稳定。
Q:磺酰氯还是磺酰氟?
如引言所述,合成化学工作者面临的一个重要问题是:能否使用特定杂芳族磺酰氯,还是应替换为更稳定(但反应活性更低)的磺酰氟。基于本文获得的结果,可提出解决这一重要问题的若干指导原则(图8):
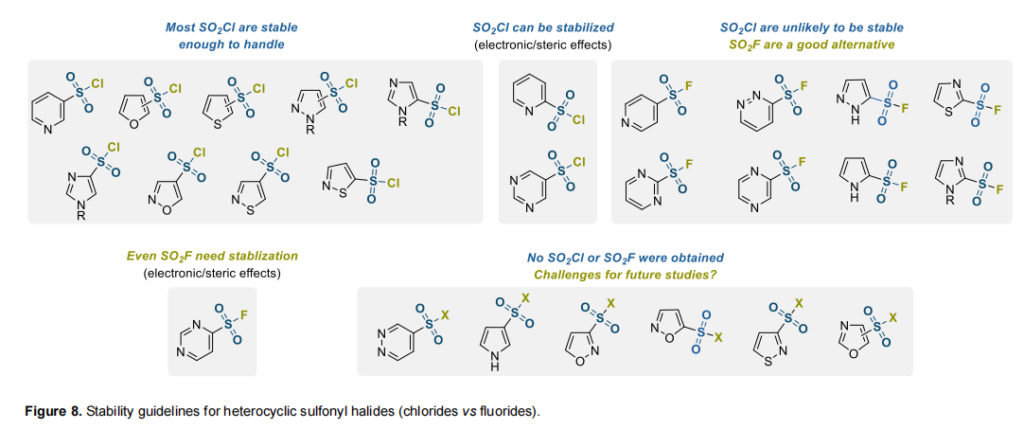
1、除少数例外,吡啶-4-磺酰氯通常不稳定,因此应使用磺酰氟。
2、吡啶-2-磺酰氯可通过吸电子取代基(尤其C-4与C-6位)以及C-6位任意基团稳定。所有其他情况下优先使用磺酰氟。
3、除少数例外,吡啶-3-磺酰氯稳定,因此无需使用磺酰氟。
4、二嗪衍生磺酰氯不稳定且无法获得,因此必须使用磺酰氟。例外包括部分嘧啶-5-磺酰氟。对于杂环部分位点(嘧啶与哒嗪的C-4原子),即使磺酰氟也需要额外稳定,例如通过额外卤素原子。
5、五元杂环磺酰氯通常对储存稳定,尽管在溶液中缓慢分解。例外包括噻唑-2-磺酰氯与吡咯-2-磺酰氯(这些情况下应使用磺酰氟),以及下一点所述磺酰卤。
6、我们无法获得以下母核唑类磺酰卤:吡咯-3-磺酰卤;异噁唑-3-磺酰卤;异噻唑-3-磺酰卤;异噁唑-5-磺酰卤;所有噁唑衍生物。部分情况下,这可能与杂环母核在磺酰卤合成条件下稳定性有限有关,而非化合物本身。
结论
杂芳族磺酰卤是化学各领域广泛使用的知名试剂,可便捷合成具有药用价值的杂环磺酰胺及其他重要化合物。与所有化学品一样,理解其稳定性对专业人员安全可靠使用至关重要。本文基于该类200余种化合物的实验数据,研究了杂芳族磺酰氯的可能分解途径。据此,我们提出简明指导原则,解决一个重要问题:特定杂环骨架能否使用磺酰氯,还是需要反应活性更低但更稳定的磺酰氟?
在杂芳族系列中,磺酰卤降解可遵循以下途径之一:(i)SO₂脱出,通常生成相应杂芳基卤;(ii)痕量水水解生成磺酸;(iii)分子中其他官能团发生反应;(iv)其他转化,通常生成复杂未知产物混合物。第一种途径常见于六元杂环磺酰氯,其中SO₂Cl基团被活化易于发生SNAr取代,且嗪氮原子具有足够亲核性。例如,母核吡啶衍生物的稳定性依次降低:β-异构体>α-异构体>γ-异构体。取代基的空间与/或电子效应若能合理针对上述因素,可提供额外稳定性。
水解分解常见于该系列最稳定的代表化合物——吡啶-3-磺酰氯以及吡唑与咪唑衍生物。嗪氮原子很可能参与水解过渡态,因此取代基的电子与空间效应也可改变相应化合物的稳定性。
若磺酰卤分子中含有易发生SNAr取代的位点(如活化硝基或卤素),水或氯离子可能在该位点发生竞争进攻,进一步使分解过程复杂化。另一重要副反应涉及含有未取代唑NH片段的五元杂环化合物的N-磺酰化。
部分情况下,磺酰氯分解生成复杂未知产物混合物,很可能因母核杂环(如呋喃、异噁唑、异噻唑)在强酸存在下稳定性有限。
上述结果使我们能够基于稳定性制定选择合适杂芳族磺酰化试剂(即磺酰氯vs磺酰氟)的指导原则。因此,吡啶-3-磺酰氯以及大多数五元杂环类似物足够稳定,可在常规化学反应中使用并库存储存。吡啶-2-磺酰氯可通过电子与空间效应稳定。吡啶-4-磺酰氯以及大多数二嗪衍生磺酰氯稳定性低,因此在这些情况下优先使用相应磺酰氟。对于部分代表化合物(包括噁唑、3-与5-取代异噁唑、3-取代异噻唑、4-取代嘧啶与吡嗪衍生物),两种磺酰卤均无法获得,这可能对未来该领域的合成研究提出挑战。
我们希望本文提出的分解途径与稳定性规律能帮助科研工作者更好理解杂芳族磺酰卤的化学,并拓展这些结构砌块在药物发现、农业化学及其他领域的应用。
本文中涉及的磺酰氯与磺酰氟化合物砌块,Enamine均有现货供应。
