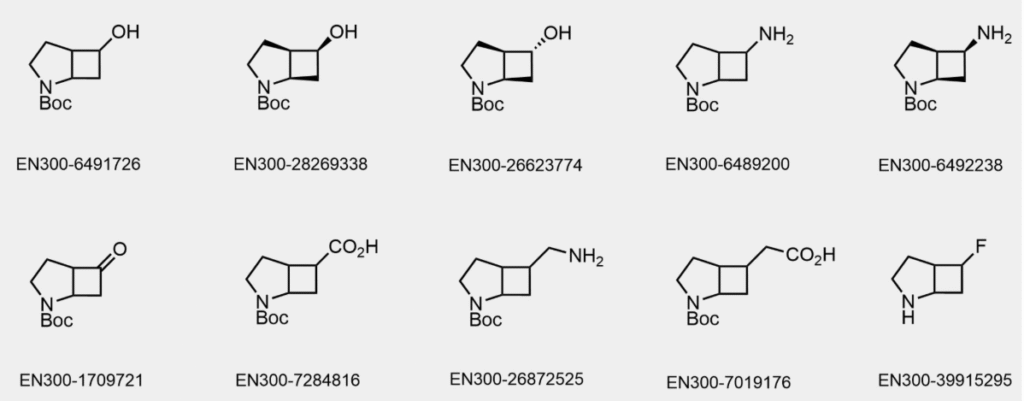
文章导读
哌啶作为药物分子中最重要的饱和环结构,其构象限制衍生的双环模拟物在药物研发中备受关注。本文报道了一种高效合成非对映纯 6-取代及 2,6-二取代 2-氮杂双环[3.2.0]庚烷砌块的新策略,核心通过 [2+2] 烯酮环加成与分子内酰胺化反应依次构建环丁烷和吡咯烷环。该方法以易获取原料为起点,无需色谱纯化,仅通过结晶即可获得单一非对映异构体产物,规模化制备量可达 30 克以上,解决了传统方法的放大难题。
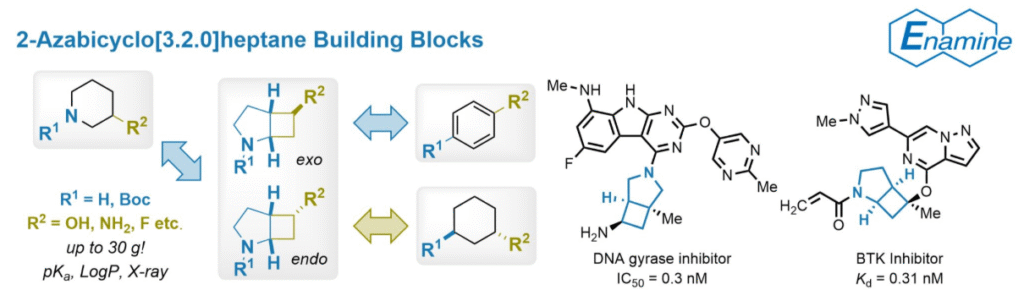
2 - 氮杂双环[3.2.0]庚烷砌块的合成及物理化学表征
本文报道了一种便捷合成非对映纯 6-取代和 2,6-二取代2-氮杂双环[3.2.0]己烷的方法。该方法基于通过 [2+2] 烯酮环加成和内酰胺形成反应,分别依次构建目标双环体系的环丁烷环和吡咯烷环。尽管关键的环加成步骤立体选择性适中(非对映异构体比例 dr=2:1),但无需色谱纯化即可获得纯非对映异构体的目标双环产物。该反应序列以易获取的起始原料为开端,且易于规模化扩大(最高可达 32.8 克)。通过制备一系列外型和内型异构氨基醇及单保护二胺(这些都是药物研发中极具价值的砌块),证实了所合成中间体的实用性。通过测定物理化学性质、进行结构研究及出口向量图分析,评估了它们在等排体取代中的潜力。
1. 引言
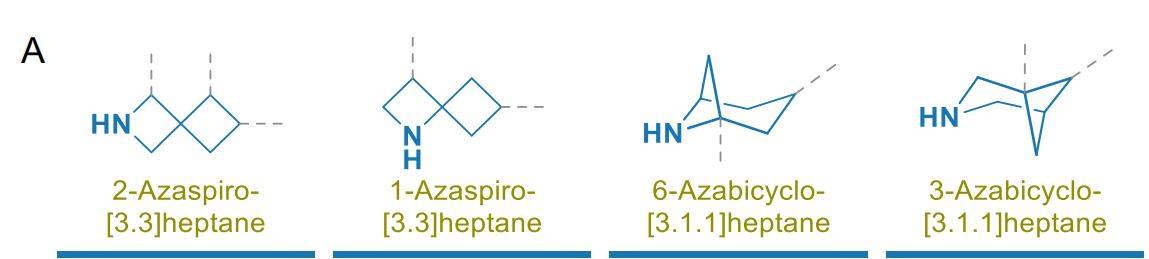
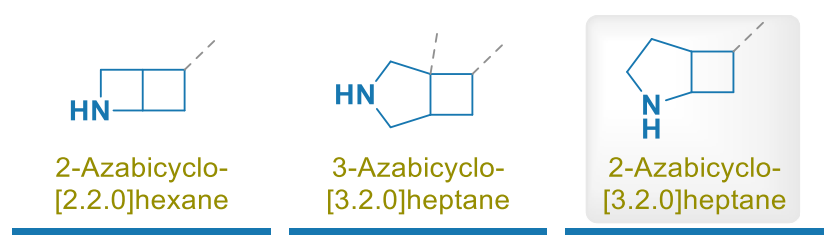
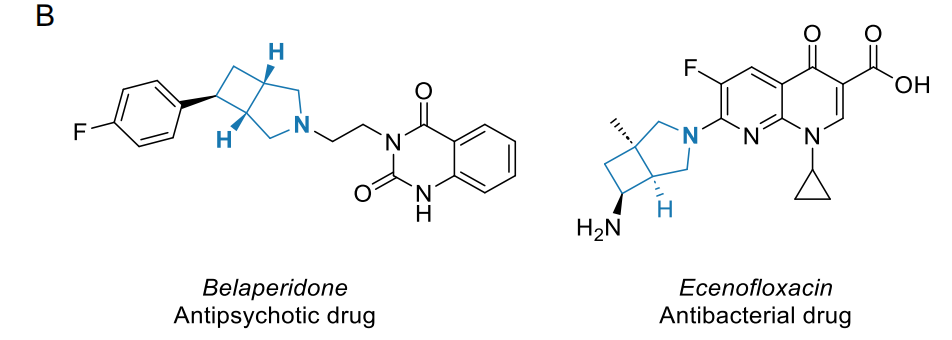
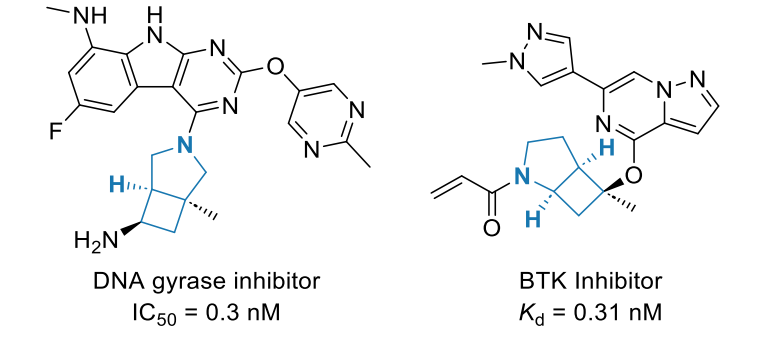
哌啶已被证实是药物分子中最重要的饱和环 [1,2],并且在众多研究中成为类似物设计的目标,主要通过构象限制实现。特别是螺环 [3-12]、桥环 [13-15] 和稠环 [16-19] 双环哌啶模拟物近年来受到了广泛关注(图 1A)。其中,3-氮杂双环 [3.2.0] 庚烷已成为研究性药物贝拉哌酮(Belaperidone,LU111995)[20] 和依诺沙星(Ecenofloxacin,CFC-222)[21] 以及处于不同研发阶段的许多其他生物活性化合物的组成部分 [22]。异构的 2-氮杂双环 [3.2.0] 庚烷在文献中报道较少,它已被用于开发高效共价布鲁顿酪氨酸激酶抑制剂 [23]。
合成 2 - 氮杂双环 [3.2.0] 庚烷的经典方法包括烯基氨基甲酸酯与烯酮 [24-27] 或其他活化烯烃 [28] 的分子间 [2+2] 环加成反应。遗憾的是,我们发现,当尝试多克级制备目标化合物时,该转化反应的产率(对于 N-Boc 保护的衍生物和原位生成的二氯烯酮而言)显著降低,并且根据核磁共振氢谱(¹H NMR)数据显示,碳酰化是主要反应过程(方案 1A)。其他值得关注的方法依赖于硝基芳烃的光化学转化 [29]、铜催化的烯炔环化反应 [30],但这些方法仅在亚克级规模下进行了评估(方案 1B、C)。
在本研究中,我们报道了一种便捷的多克级制备 6-官能化 2-氮杂双环 [3.2.0] 庚烷 1(作为有前景的哌啶模拟物)的方法。我们的合成策略基于通过分子内酰胺形成反应,将吡咯烷环稠合到适当官能化的环丁烷衍生物 3 上,而环丁烷衍生物 3 本身则通过烯酮 [2+2] 环加成反应获得(方案 1D)。我们还对标题骨架进行了结构和物理化学评估,以阐明其在等排体取代中的潜力。
2. 结果与讨论
2.1 合成
如上所述,我们制备目标双环体系的逆合成方法基于在适当三官能化的环丁烷衍生物 3 中进行分子内酰胺形成反应(方案 1D)。该方案的瓶颈在于该关键中间体需要特定的立体化学结构以确保环化反应成功进行。
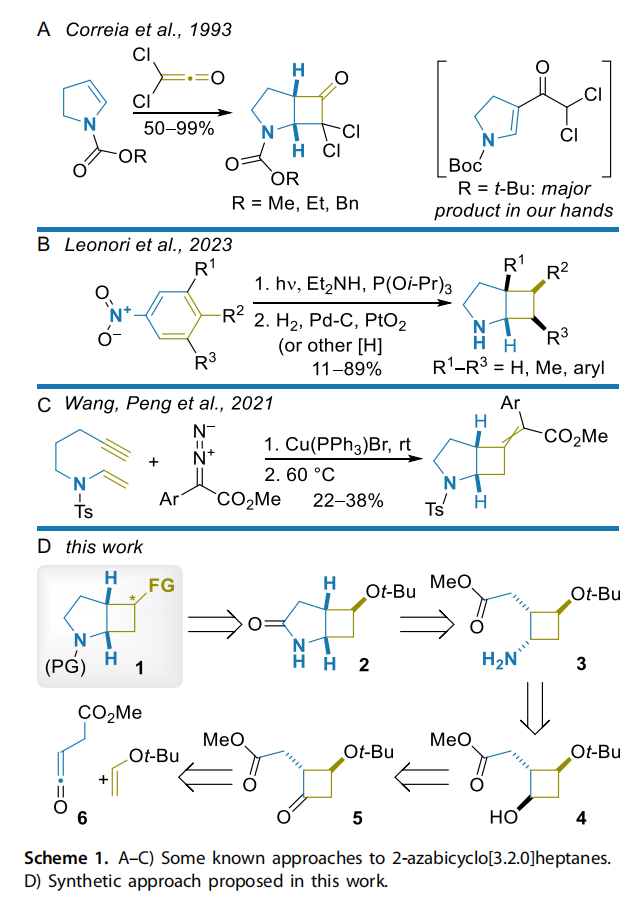
我们期望通过一些涉及醇 4 或其衍生物的双分子亲核取代(S_N2)反应(例如通过中间体叠氮化物的形成)在化合物 3 的分子中引入氨基。反过来,酮 5 的还原可能会提供具有所需立体化学结构的醇 3。最后,化合物 5 的环丁烷环可以通过烷基乙烯基醚与烯酮 6 的 [2+2] 环加成反应轻松构建,而烯酮 6 本身则由易获取的 4-氯- 4-氧代丁酸甲酯(8)原位生成。
尽管所提出的合成方案中多达三步反应(6→5、5→4 和 4→3)存在非对映选择性问题,但我们仍决定冒险实施该方案,期望能够利用目标内酰胺 2 与其他副产物在物理性质上的差异将其分离。选择叔丁基作为起始乙烯基醚中羟基部分的保护基,原因是其在酸的作用下易于脱保护,且其空间位阻可能有助于解决立体化学问题(方案 2)。反应序列的第一步在产物产率和规模化方面非常高效(产率 70%,最高可获得 114 克化合物 5),但反式非对映选择性适中(dr=2:1)。酮 5 在四氢呋喃-水(THF-H₂O)混合溶剂中与硼氢化钠(NaBH₄)反应生成醇 4。除目标化合物 4 外,反应混合物中还生成了另一种副产物(9)。尽管我们无法分离这些化合物,但所有可用的光谱数据均证实了化合物 9 为内酯结构(详见支持信息)。化合物 9 的形成可以通过醇 4 的全顺式非对映异构体的环化反应来解释。无需纯化中间体,直接将化合物 4 和 9 的混合物进行甲磺酰化、与叠氮化物反应及催化氢化。令我们非常满意的是,化合物 3 的(1S*,2S*,4S*)非对映异构体(如方案 1D 所示)自发环化生成目标内酰胺 2(具有(1S*,5S*,6S*)或外型构型),该产物为晶体(熔点 118-120℃),可通过己烷研磨轻松分离。包括化合物 9 在内的所有其他组分均留在溶液中并被弃去,而目标产物 2 的总产率为 33%。通过核磁共振(NMR)实验证实了化合物 2、4、5 和 10(混合物中的关键非对映异构体)的相对立体化学结构(详见支持信息)。
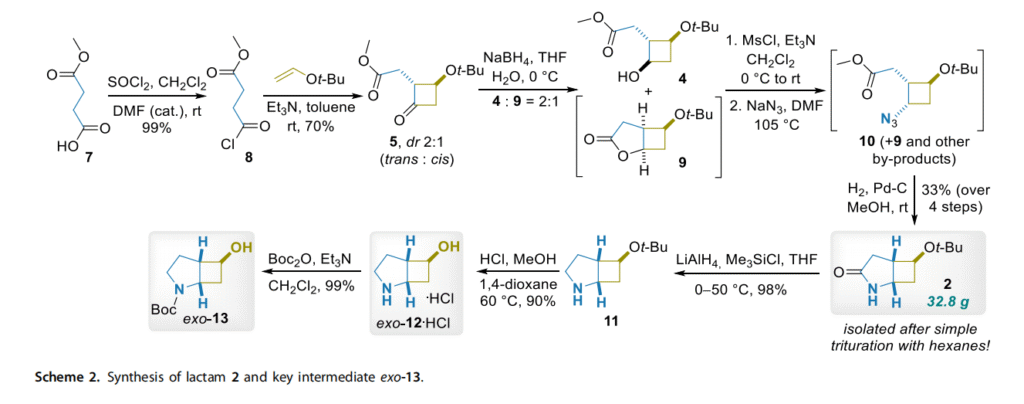
使用四氢铝锂-三甲基氯硅烷(LiAlH₄-Me₃SiCl)还原内酰胺 2,几乎定量地获得了氨基醇 11。在 60℃下,化合物 11 在 1,4-二氧六环-甲醇混合溶剂中与 4M 盐酸(HCl)反应进行氧脱保护,以 90% 的产率得到氨基醇外型-12(盐酸盐形式)。经过 N-Boc 保护后,几乎定量地获得了衍生物外型-13。
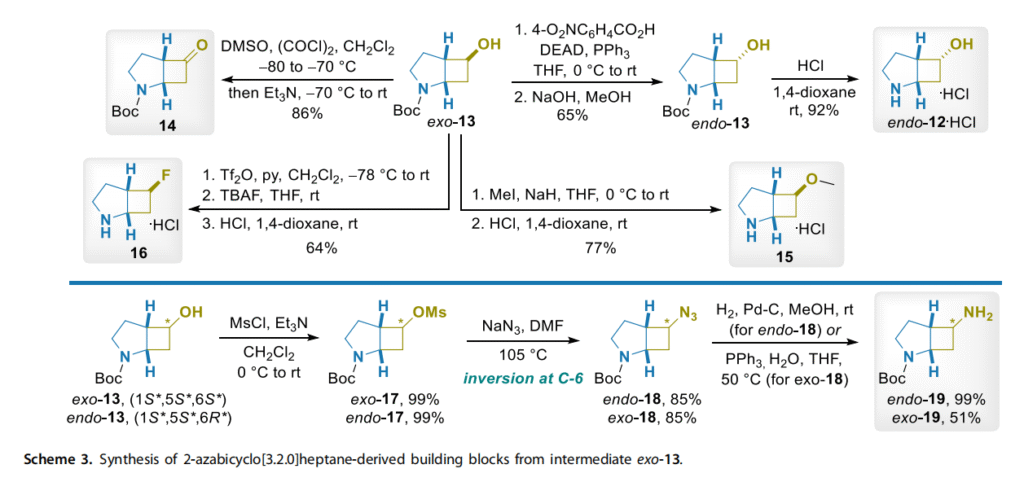
化合物外型-13 是合成一系列其他具有合成价值的 2-氮杂双环 [3.2.0] 庚烷衍生砌块的关键中间体(方案 3)。具体而言,通过形成相应的 4-硝基苯甲酸酯进行Mitsunobu构型翻转,得到非对映异构衍生物内型-13(两步反应产率 65%),脱保护后获得氨基醇内型-12(盐酸盐形式,产率 92%)。醇外型-13 经Swern氧化得到酮 14a(产率 86%),而氧甲氧基化后再进行 N-脱保护得到盐酸盐 15(两步反应产率 77%)。外型-13 经脱氧氟化后再进行 N-脱保护得到单氟化胺盐酸盐 16(两步反应产率 64%)。值得注意的是,脱氧氟化步骤在 C-6 原子处保持了构型,这可能与氮原子的参与有关(这在 3-取代哌啶中是众所周知的 [31])。外型-13 和内型-13 均经过甲磺酰化、与叠氮化物的 S_N2 反应及还原反应,分别以三步反应产率 83% 和 43% 得到 N-Boc-单保护二胺内型-19 和外型-19。
2.2 物理化学和结构表征
为了阐明 2-氮杂双环 [3.2.0] 庚烷在药物化学中等排体取代中的潜力,我们测定了其模型衍生物的物理化学性质(即 pKa 和分配系数 LogP)并进行了 X 射线衍射研究。因此,对盐酸盐外型-12・HCl、内型- 12・HCl 和 3-羟基哌啶进行标准水相酸碱滴定,结果表明双环骨架对化合物的酸碱性质影响较小(图 2A)。两种双环氨基醇的碱性均略低于相应的单环类似物。对于内型异构体,差异小于实验误差(0.07-0.14),而对于外型-12,ΔpKa 值为 0.18-0.14。
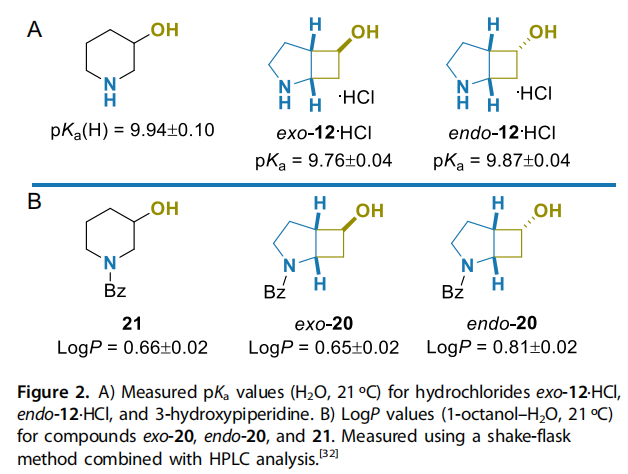
对于分配系数(LogP)的测定 [32],合成了 N-苯甲酰基衍生物外型-20、内型-20 和 21(图 2B;详见实验部分)。结果发现,尽管外型异构体外型-20 的分子中多了一个碳原子,但其亲脂性与 3-羟基哌啶衍生物 6 几乎相同(LogP 值分别为 0.65±0.02 和 0.66±0.02),而内型-20 的亲脂性高出 0.15-0.04 个单位。一种可能的解释是内型-20 分子中羟基的溶剂可及性较低。
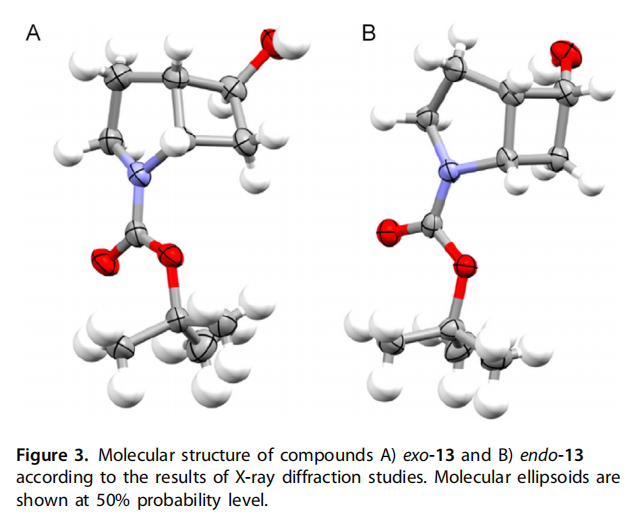
对化合物外型-13 和内型-13 进行了 X 射线衍射研究(图 3)。为了评估标题骨架的三维结构,使用了出口向量图(EVP)分析 [33,34]。出口向量图(EVP)工具基于将二取代骨架表示为两个出口向量 n₁和 n₂,这两个向量由连接到相应环系的取代基定义(图 4A)。这些向量的相对取向可以通过四个几何参数明确描述:起始点之间的距离 r、平面角 φ₁和 φ₂以及二面角 θ(图 4B)。通过在 r-θ、θ-φ₁/φ₂或 φ₁-φ₂坐标中描绘目标骨架,可以获得出口向量图(EVP)。在我们之前的研究中,我们对单环二取代骨架在这些坐标中覆盖的化学空间进行了全面分析,并确定了此类环系可访问的几个出口向量图(EVP)区域(α-ε)[33,34]。任何新的骨架都可以与这些区域进行比较,以获得其作为药物化学中潜在等排体应用的结构见解。
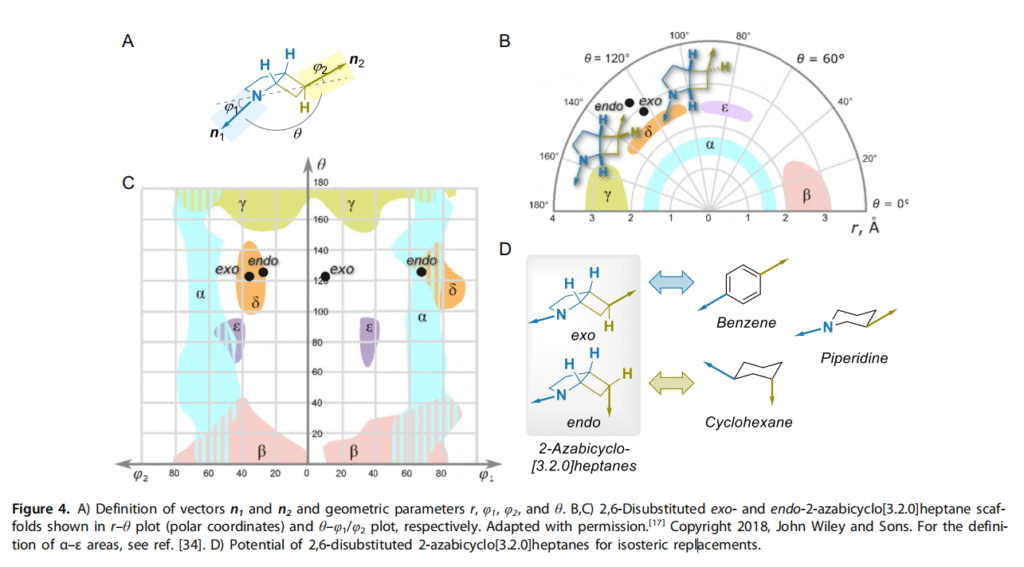
基于 X 射线衍射研究的结果,我们获得了非对映异构(即外型和内型)2,6-二取代 2-氮杂双环 [3.2.0] 庚烷骨架的 r、φ₁、φ₂和 θ 参数值(图 4A)。结果发现,这两种骨架均采用了哌啶不常见的构象。相反,它们位于反式-1,3-二取代环己烷特有的 δ 区域附近(r=2.50-2.56Å,φ₁=64°-88°,φ₂=29°-39°,θ=93°-124°)(图 4B、C)。本研究中所研究的两种双环骨架都稍大一些(外型和内型异构体的 r 值分别为 2.94Å 和 3.21Å)。主要差异在于外型异构体的 φ₁值(φ₁=9°,φ₂=36°,θ=123°),这表明与母体环烷烃相比,该骨架明显扁平化。φ₁和 φ₂角的相对较小值对应于出口向量 n₁和 n₂的近乎共线取向。对于这种分子几何结构,θ 参数的值没有意义,因为即使是微小的结构变化也会导致相应二面角的显著变化。同时,共线出口向量取向是 1,4-二取代苯的特征(其中 r=2.80Å,φ₁=φ₂=0°);在这种情况下,根本无法定义 θ 角。该结果表明,外型-2,6-二取代 2-氮杂双环 [3.2.0] 庚烷可以被视为扭曲的富含 sp³ 杂化的苯等排体。对于内型异构体,在角度参数方面与反式-1,3-二取代环己烷的结构相似性非常明显(φ₁=66°,φ₂=27°,θ=125°)。
3. 结论
在本研究中,我们提出 2,6-二取代 2-氮杂双环 [3.2.0] 庚烷骨架作为一种重要的化学型,可用于早期药物研发项目的各种应用。标题双环核心可以通过依次构建环丁烷环和吡咯烷环,以直接高效的方式获得。叔丁基乙烯基醚与由丁二酰氯甲酯生成的烯酮的 [2+2] 环加成反应,以及分子内酰胺化反应,是实现目标体系合成的关键步骤。尽管环加成反应的非对映选择性适中(dr=2:1),并且当在三取代环丁烷中间体中引入第三个手性中心时,立体化学问题变得更加突出,但仅使用结晶作为纯化技术,即可获得单一外型非对映异构体的目标双环内酰胺。这一事实以及起始原料的高可获得性,使得该方案易于规模化扩大(最高可达 30 克),并且能够以 7-12 步总产率 9%-20% 制备对药物研发有价值的外型和内型异构饱和双环砌块(即单保护二胺和氨基醇)。
为了评估 2,6-二取代 2-氮杂双环 [3.2.0] 庚烷骨架在药物化学中等排体取代中的潜力,我们对其进行了物理化学和结构研究。因此,与母体 3-羟基哌啶相比,相应双环氨基醇盐酸盐的 pKa 值仅因双环体系而略有降低,并且这种影响对于外型异构体更为明显。尽管双环体系中增加了一个碳原子,但外型异构模型苯甲酰胺的亲脂性与 3-羟基哌啶衍生物基本相同。相反,内型异构体的亲脂性略高,这可能是由于羟基的溶剂可及性较低。
基于 X 射线衍射研究获得的实验数据,对标题双环骨架进行的出口向量图(EVP)分析表明,外型和内型异构骨架均与反式-1,3-二取代环己烷具有相似性,尽管尺寸稍大(图 4D)。内型异构体在角度参数方面与上述骨架具有高度相似性,而外型异构体则明显扁平化,因此可以预期其作为 1,4-二取代苯的扭曲三维类似物具有出人意料的潜在应用 [35]。
4. 实验部分
略
如需查阅研究全文、详细实验流程及支持资料,可访问:https://doi.org/10.1002/ejoc.202500970,文中提及的各类中间体和最终产物均可在 Enamine 购买。