编者按:氮杂环丁烷环是药物研发的 “明星结构”,现有 7 种获批药物含该单元,数十种相关分子进入临床,但其 2 - 取代异构体的规模化合成长期是难题。文章发表于《Organic Letters》2025 年第 27 卷,由 Enamine 公司与辉瑞(Pfizer)团队合作完成,以光化学为核心,让氮杂环丁烷- 2-羧酸与烯烃直接官能团化,既填补 2-烷基氮杂环丁烷合成空白,更实现多重突破——兼容批次与流动化学,覆盖毫克至多克级制备,流动反应单次可获 48g 产物;还能合成磺酰氟、磷酸二甲酯等创新砌块,契合药物研发核心需求。这项研究不仅为 2-烷基氮杂环丁烷提供 “新解法”,更彰显光化学在药物合成中的潜力,为医药化学创新注入新动力。
通过间歇式与流动式光化学方法合成烷基氮杂环丁烷
摘要
以氮杂环丁烷-2-羧酸为原料,通过间歇式与流动式光化学修饰反应,成功制备出烷基氮杂环丁烷。该反应可实现毫克级、克级至多克级规模制备,所得氮杂环丁烷是药物研发领域中极具价值的合成砌块。
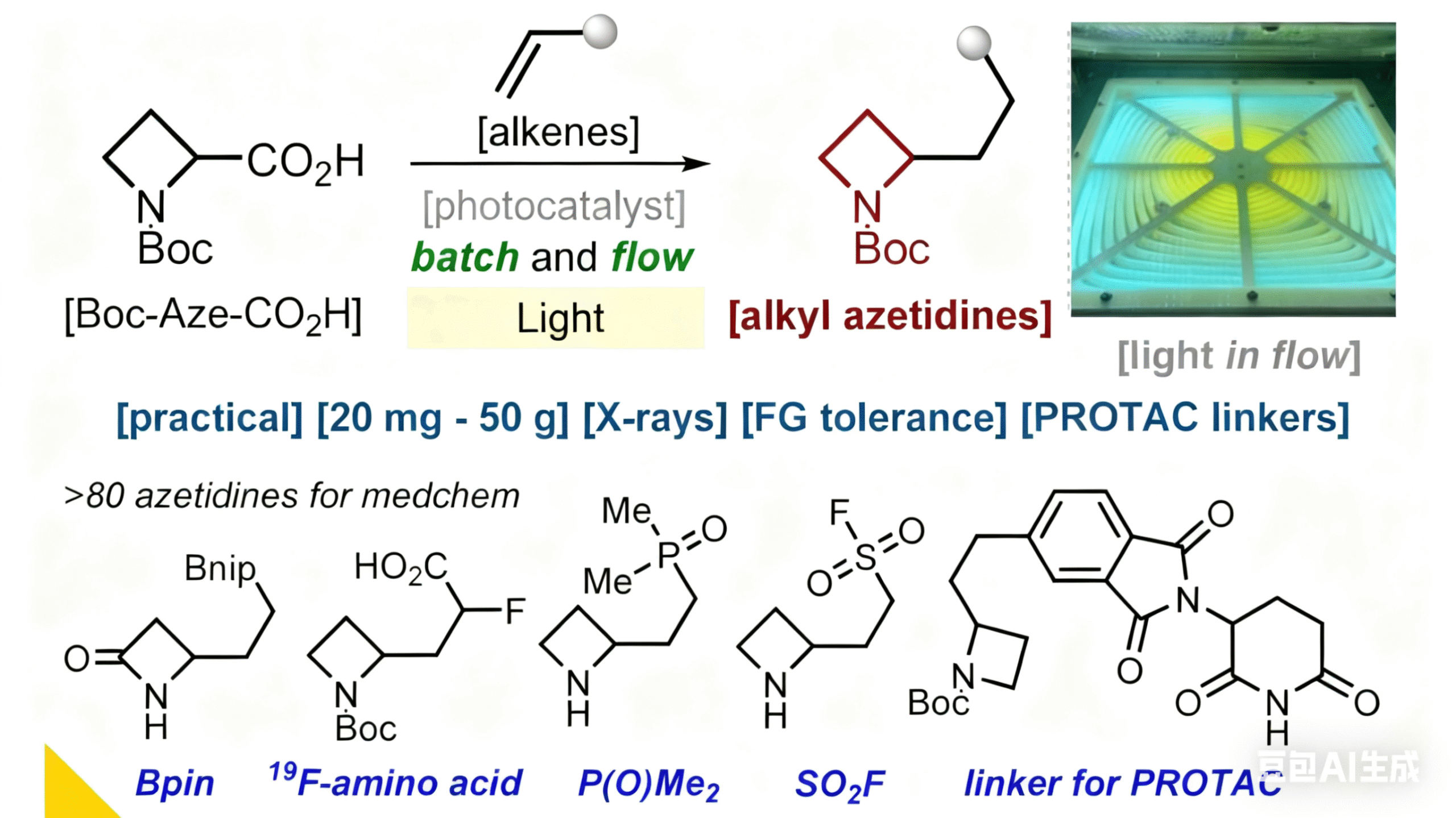
引言
过去十年间,氮杂环丁烷环在药物研发领域的应用日益广泛。目前,至少有 7 种已获批药物含有氮杂环丁烷结构单元,另有数十种含氮杂环丁烷结构的生物活性分子正处于不同阶段的临床试验中 [1]。要进一步推广这一结构单元的应用,亟需开发新型合成方法,以获得功能更丰富多样的合成砌块。
因此,科研人员在制备取代氮杂环丁烷方面投入了大量精力 [2]。然而,现有方法大多聚焦于 3 - 取代氮杂环丁烷的合成 [2,3],2-取代氮杂环丁烷的合成方法则较为罕见 [4]。
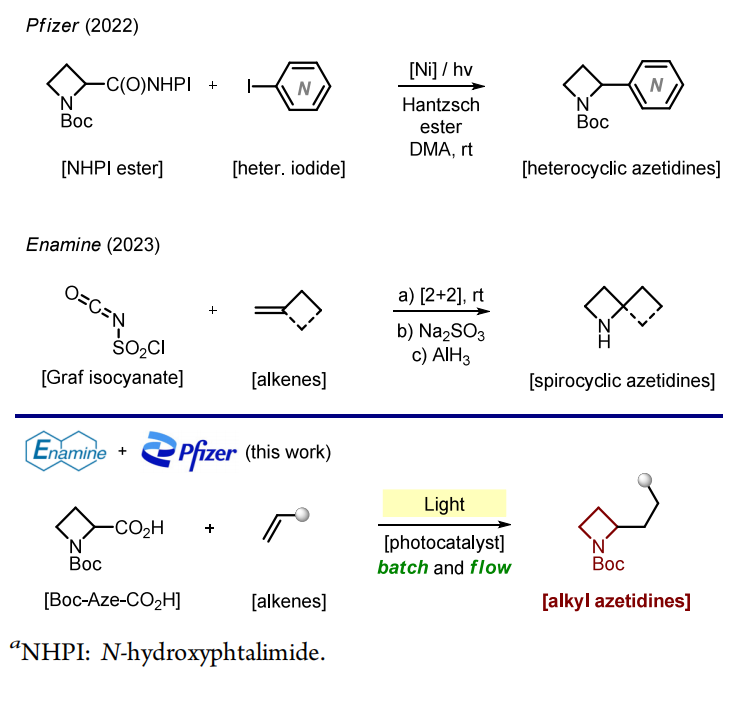
本实验室一直致力于开发多种策略,以合成药物化学领域所需的多取代氮杂环丁烷。例如,2022 年,辉瑞(Pfizer)公司报道了通过镍(Ni)催化含氮杂环丁烷的氧化还原活性酯脱羧(杂)芳基化反应,制备 2-(杂)芳基氮杂环丁烷(方案 1)[5];2023 年,Enamine 公司以格拉夫异氰酸酯(Graf isocyanate)与环外烯烃的形式 [2+2] 环加成反应为基础,开发出2-螺环氮杂环丁烷的实用合成方法(方案 1)[6]。
本文报道了 Enamine 公司与辉瑞公司的合作研究成果:以氮杂环丁烷-2-羧酸与烯烃为原料,通过直接光化学修饰反应制备烷基氮杂环丁烷。该反应可通过间歇式和流动式两种方式实现,能够以毫克级、克级至多克级规模制备药物化学领域所需的烷基氮杂环丁烷。这是首个针对该主题的系统性研究。
方案 1. 药物化学领域中 2-取代氮杂环丁烷的制备:前人研究与本研究
方案 2. 反应条件优化
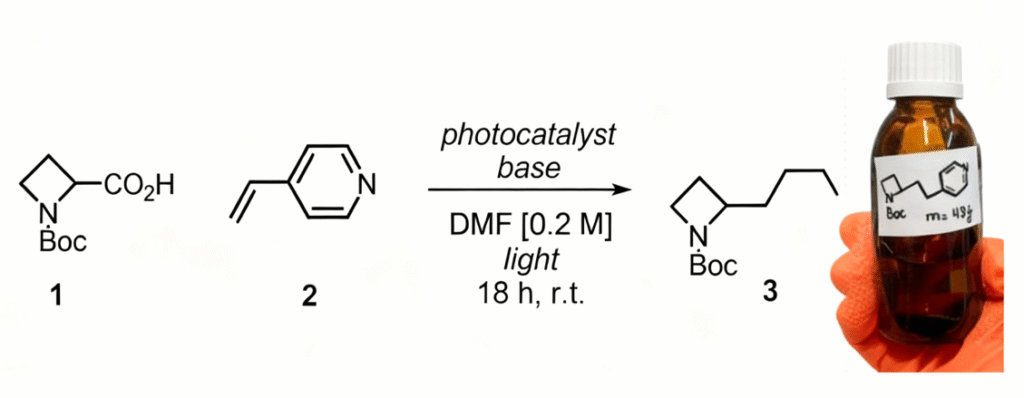

a 间歇式合成:氮杂环丁烷羧酸 1(150 毫克,745 微摩尔,1.0 当量)、4-乙烯基吡啶 2(157 毫克,1.49 毫摩尔,2.0 当量)、光催化剂(2.5 摩尔 %,18.6 微摩尔)、一水合氢氧化锂(34.4 毫克,820 微摩尔,1.1 当量),溶于 DMF(0.2 mol/L)中。经高效液相色谱(HPLC)纯化后得到分离产率。(a) 365 nm 光源;(b) 450 nm 光源;(c) 660 nm 光源。流动式合成:氮杂环丁烷羧酸 1(1.0 当量)、4-乙烯基吡啶 2(1.5 当量)、4CzIPN(2.0 摩尔 %)、一水合氢氧化锂(1.1 当量),溶于 DMF(0.2 mol/L)中,365 nm 光源照射,流速 30 毫升 / 分钟。BTMG:1,1,3,3 - 四甲基胍;PMP:对甲氧基苯基;n.d.:未检测到。
反应条件优化
氨基酸与烯烃的光化学反应此前已有报道 [7,8],但令人意外的是,含氮杂环丁烷结构的底物并未出现在这些研究中。另一方面,在各类自由基反应中,含氮杂环丁烷的化合物仅以非系统性的方式少量生成 [9,10]。因此,我们以市售的 Boc 保护氮杂环丁烷 -2-羧酸(1)与市售的迈克尔受体 4-乙烯基吡啶(2)为原料,开展直接光化学反应条件的探索。通过改变碱、光催化剂和光源波长,确定了最佳反应条件(方案 1)。
研究发现,在二甲基甲酰胺(DMF)中,以 Ir [dF (CF₃) ppy]₂(dtbpy) PF₆为光催化剂、450 nm 光照射下,氮杂环丁烷 1 与乙烯基吡啶在多种碱存在下均可发生反应:使用碳酸钾(方案 2,序号 1)、2-叔丁基-1,1,3,3-四甲基胍(序号 2)、磷酸三钾(序号 3)和一水合氢氧化锂(序号 4)时,产率分别为 39%、30%、<25% 和 76%。使用 2,4,6-三甲基吡啶时,未检测到目标产物(序号 5)。将金属配合物光催化剂替换为有机光催化剂 4CzIPN,并在 365 nm 光照射下反应(序号 6),仍能以 66% 的合理产率得到产物 3。尝试进一步更换光催化剂为 TiO₂锐钛矿(序号 7)、Ru(bpy)₃Cl₂(序号 8)、吖啶盐光催化剂(序号 9-11)和锇(II)配合物催化剂(序号 12-13)时,仅得到极少量目标产物或未检测到产物。为替换 DMF 而进行的溶剂筛选结果显示,使用四氢呋喃(THF)和乙腈时,反应产率均有所下降。对照实验表明,无光照条件下反应无法进行(序号 14、15)。
放大合成
此前,我们已将流动式光化学方法应用于药物化学领域所需的双环 [1.1.1] 戊烷的多克级制备 [11]。本研究中,我们希望将这一技术应用于烷基氮杂环丁烷的多克级合成。因此,在确定最佳间歇式反应条件(序号 4 和 6)后,我们采用成本更低的有机催化剂 4CzIPN,通过流动式反应进行放大(序号 16)。令人满意的是,在此条件下,单次反应即可轻松得到 48 克产物 3,产率为 61%(方案 2)。
反应范围
在获得优化反应条件后,我们进一步探索了该反应在合成多取代氮杂环丁烷中的应用(方案 3)。在考察反应范围时,间歇式反应中可灵活选用金属铱(Ir)配合物或有机催化剂 4CzIPN;多种氮杂环丁烷产物后续也通过流动式反应,以有机催化剂实现了规模化制备。
方案 3. 反应范围:烯烃的多样性及氮杂环丁烷环上的取代反应。


多种杂芳基苯乙烯(如 2 - 乙烯基吡啶、2 - 乙烯基嘧啶、2 - 乙烯基吡嗪及相应的乙烯基噻唑)均可参与加成反应,生成氮杂环丁烷 4-7,产率为 55%-74%。取代苯乙烯同样能顺利反应,以良好产率得到相应的氮杂环丁烷 9-12。为验证该反应的应用潜力,我们还考察了其与 5 - 乙烯基沙利度胺的反应,生成了新型 E3 泛素连接酶招募剂合成砌块 13,产率为 28%。更传统的迈克尔受体(如丙烯酸甲酯、甲基乙烯基酮等)可生成氮杂环丁烷 14-20,产率为 47%-70%。
氮杂环丁烷-2-羧酸与CH₂=CHSO₂F反应生成产物 21。据我们所知,这是首次以非活化氨基酸为原料直接制备磺酰氟的实例 [12]。
与乙烯基砜、丙烯腈及含 PO (OEt)₂基团的烯烃反应,可得到相应的氮杂环丁烷 22-26,产率为 29%-53%。PO (OEt)₂基团在已获批药物中较为常见,从这一角度看,含 MeSO₂取代基的产物 22 具有特殊研究价值。砜类化合物 24 的结构已通过 X 射线分析得到证实。值得注意的是,本研究还实现了含 PO (O) Me₂基团的氮杂环丁烷 27 的合成。2017 年,美国食品药品监督管理局(FDA)批准了抗癌药物布加替尼(Brigatinib)[14],此后,含 P (O) Me₂基团的合成砌块在药物化学研究中变得日益普遍 [15]。
与乙烯基硼酸酯反应可生成含 Bpin(频哪醇硼酸酯)基团的氮杂环丁烷 28 和 29,产率为 34%-45%。
多种含脂肪族和醚类官能团的取代 N-Boc 氮杂环丁烷 - 2 - 羧酸也适用于该反应,生成氮杂环丁烷 30-36,产率为 36%-80%。有趣的是,季碳氮杂环丁烷 - 2 - 羧酸与 4 - 乙烯基吡啶可直接发生脱羧反应,顺利生成产物 37 和 38,产率分别高达 96% 和 92%。
反应局限性
该 2-烷基氮杂环丁烷的合成方法并非毫无局限性。在以下情况下,反应无法获得良好产率:(a) 本身具有空间位阻的 β- 取代丙烯酸酯(如 MeCH=CHCO₂Me、Me₂C=CHCO₂Me);(b) 非极性烯烃(如 N-苄基马来酰亚胺、丁二烯砜);(c) 富电子烯烃(如 EtOCH=CH₂、2-噻吩基-CH=CH₂)。非反应性烯烃的完整列表详见支持信息第 30 页。富电子烯烃无法反应的现象表明,中间体N-Boc氮杂环丁烷自由基具有亲核特性 [16]。
官能团化修饰
在建立实用且可规模化的2-烷基氮杂环丁烷合成方案后,我们将多种产物转化为药物化学领域所需的高附加值、多功能含氮杂环丁烷合成砌块(含一个或两个官能团的化合物)。
方案 4. 药物化学用含氮杂环丁烷结构合成砌块的合成
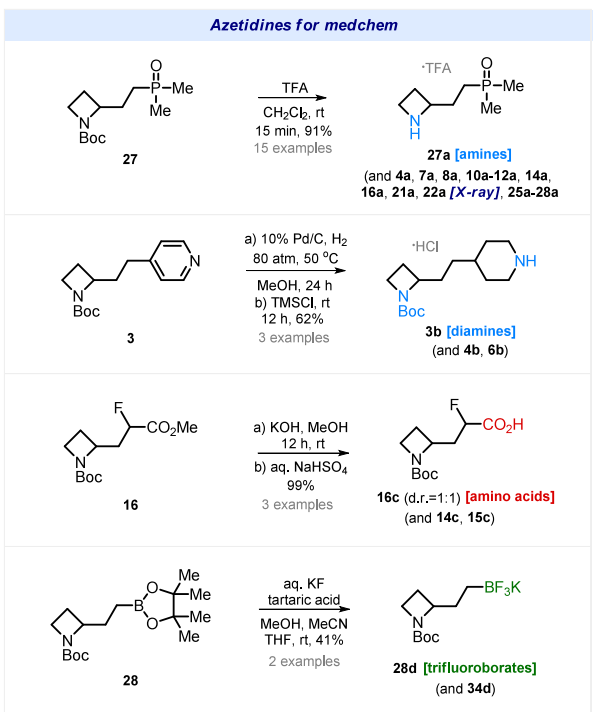
通过标准酸性条件下的 N-Boc 脱保护反应,可得到胺类化合物 “a”(方案 4)。胺类化合物 22a 的结构已通过 X 射线分析证实。在甲醇中,通过 H₂/Pd 催化加热,对吡啶 / 吡嗪环进行还原,可得到二胺类化合物 “b”。
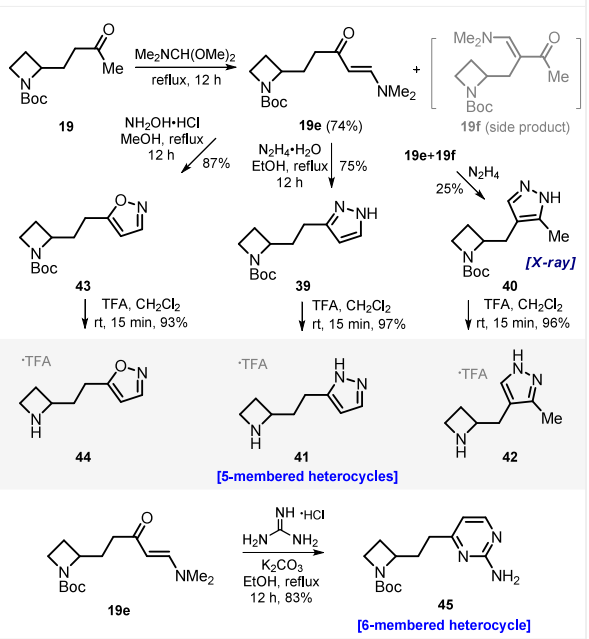
酯基皂化反应可生成具有研究价值的氨基酸类化合物 “c”。含 Bpin 基团的化合物与氟化钾在丙酮/ 水混合体系中反应,可顺利生成三氟硼酸钾类化合物 “d”。化合物 19 与 Me₂NCH (OMe)₂反应,生成两种异构体混合物(19e:19f=3:1),通过柱层析分离可得到纯异构体 19e,产率为 74%。19e 与水合肼环合反应生成吡唑 39,产率为 75%;19e 与 19f 的混合物与水合肼反应后,经柱层析分离异构体,可得到吡唑异构体 40,其结构已通过 X 射线分析证实。N-Boc 基团经酸性脱保护后,生成独特的异构体骨架 41 和 42。19e 与羟胺环合反应可生成异噁唑 43,产率为 87%;异噁唑 43 经酸性 N-Boc 脱保护后,得到骨架化合物 44。化合物 19e 与胍缩合反应可顺利生成嘧啶 45,产率为 83%。
结论
本研究开发了一套统一的反应条件,实现了氮杂环丁烷-2-羧酸与烯烃的直接光化学官能团化反应。该反应可通过间歇式和流动式两种方式进行,能够快速以毫克级、克级至多克级规模制备烷基氮杂环丁烷。所得产物(如磺酰氟、频哪醇硼酸酯、三氟硼酸钾、含 PO (O) Me₂基团的衍生物、PROTAC 连接子等)是药物研发领域极具价值的合成砌块。
