1、摘要
本文提出一种可靠的方法,可多克级制备非对映体富集的3,6-二取代双环[3.2.0]庚烷结构砌块。该策略基3-取代环戊烯衍生物与二氯烯酮的[2+2]环加成,随后进行非对映选择性还原。尽管两步均不具有立体专一性,仍可以纯非对映体形式获得目标外消旋双环砌块(包括氨基酸与氨基醇),规模最高可达34.4克。利用出口矢量图(EVP)对目标骨架进行结构表征,结果表明其在药物化学中可作为环烷烃/苯环的电子等排体替代单元。
2、引言
饱和双环骨架在药物发现中受到广泛关注,因其可赋予衍生物丰富且可预测的三维分子形状。这类骨架也符合当前药物化学推崇的高sp³杂化、低分子量、理化性质可控的设计理念。饱和双环骨架已成为简单环系(如环烷烃、苯环)的重要电子等排替代物。已有研究表明,核心骨架的几何形状对生物活性分子的整体构象至关重要,同时在不对称催化剂设计中,配体形状也直接决定反应选择性。
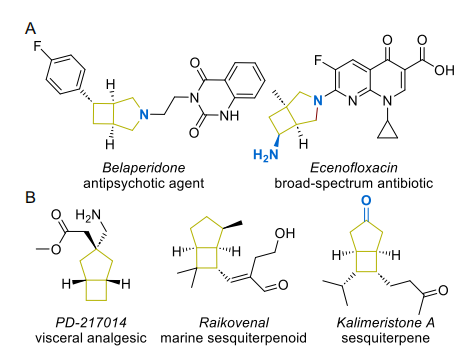
在众多饱和双环化合物中,双环[3.2.0]庚烷衍生物尤为突出。多数研究集中于氮杂双环体系,药物候选物贝拉哌酮(Belaperidone)与依诺沙星(Ecenofloxacin)是药物化学中最具代表性的案例。母核双环烃骨架虽已被发现超60年,但因缺乏高效构建方法,长期未被药物化学家重视。代表性案例包括辉瑞开发的强效内脏镇痛药PD-217014,以及多种萜类天然产物。双环[3.2.0]庚烷衍生物也作为不对称催化配体受到合成化学家关注。
本工作聚焦3,6-双官能化双环[3.2.0]庚烷(1)——一类高sp³杂化、三维结构丰富,且极具环烷烃/苯环等排体潜力的砌块。
已知制备方法包括:
3-羟基庚-6-烯酸分子内环化串联反应
环庚三烯醇光化学异构
三环-[3.2.0.02,7] 庚-3-酮酸催化重排
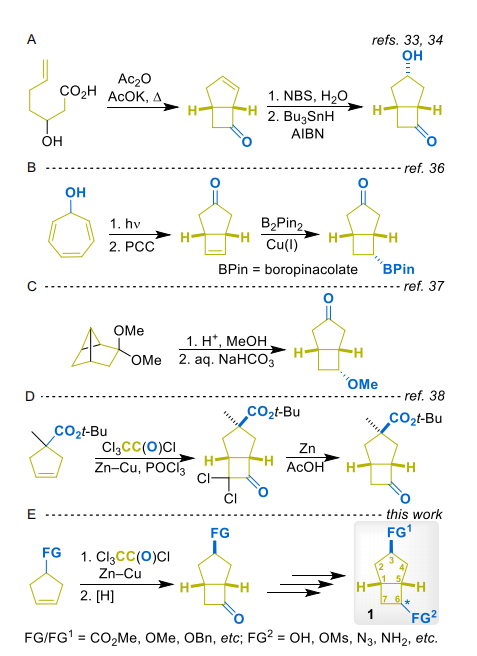
这些方法普遍存在原料难获取、关键步骤使用有毒试剂等问题,难以广泛应用。Greene等在天然产物hirsutic acid C全合成中报道了一种简洁路线:以环戊-3-烯-1-羧酸酯与二氯烯酮进行[2+2]环加成构建目标骨架。
本工作沿用该思路,实现多种3,6-双官能化双环[3.2.0]庚烷(1)的多克级合成。鉴于目标分子含4个手性中心,本研究重点关注非对映选择性制备,并通过X射线衍射(XRD)对所得非对映异构骨架进行结构表征,评估其在药物发现中作为电子等排体的潜力。
3、结果与讨论
3.1 [2+2]环加成与还原脱氯优化
以商品化环戊烯衍生物(2a–c)与二氯烯酮为起始,对[2+2]环加成进行优化。
● 溶剂由乙醚改为1,4-二氧六环,无需添加POCl₃
● 还原剂由锌-铜偶改为锌粉,操作大幅简化
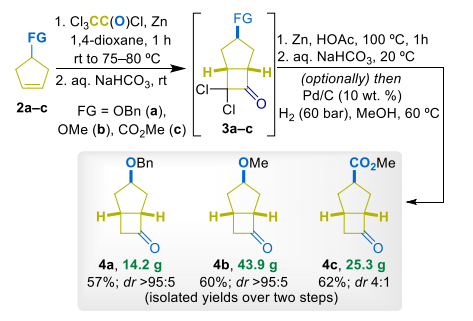
改进后反应快速、平稳得到二氯酮中间体(3a–c)。该中间体稳定性差,无需纯化直接投料。经锌粉介导的还原脱氯,以57%–62%总收率得到3-官能化酮(4a–c),非对映选择性良好:
● 4a/4b:dr > 95:5
● 4c:dr = 4:1
脱氯步骤对温度敏感,100℃以下无法完全转化;未完全还原产物可通过高压釜Pd催化氢解转化为目标酮。
● 单次反应规模最高可达43.9克
● 分批并行放大可制备71克4a
4c的endo/exo异构体无法分离,以混合物形式用于后续转化。底物2c的非对映选择性偏低,可能源于酯基吸电子效应导致双键反应性降低、环加成活化能升高,需在更高温度引发,从而降低选择性。
3.2 构型确证(NOE)
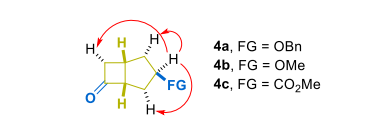
酮类产物(4a–c,主非对映体)的相对构型通过NOE实验确证:
选择性激发H-3质子,可观察到与2-、4-、7-亚甲基质子的相关信号,而与H-1、H-5无相关,证明C-3取代基为exo构型。
3.3 立体选择性还原与衍生化
酮 4a、4c 为关键中间体。
● NaBH₄还原4a无立体选择性,非对映体比例约1:1
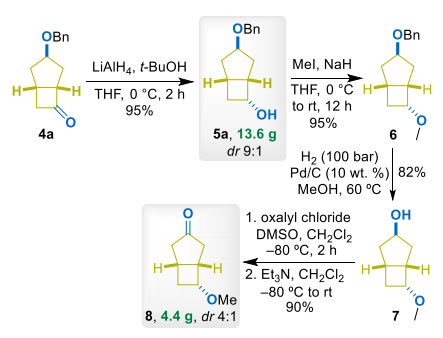
● 改用Li[AlH(Ot-Bu)₃](原位由LiAlH₄与叔丁醇制备),可高立体选择性得到exo,endo-5a,dr=9:1
由醇5a出发,经甲基化、氢解脱苄、Swern氧化得到酮8,非对映选择性略有下降(dr=4:1),可能与纯化过程中少量次要异构体富集有关。
3.4 氨基醇与氨基酸砌块合成
(1)氨基醇合成
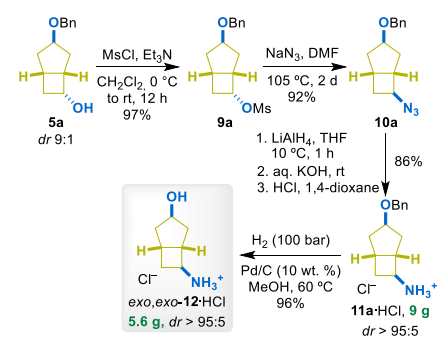
醇5a经甲磺酰化、叠氮化(Sₙ2构型翻转)、LiAlH₄还原得到胺11a,成盐后在乙腈/异丙醇中重结晶,非对映纯度提升至dr>95:5;催化氢解脱苄得到目标氨基醇exo,exo-12(盐酸盐)。
(2)氨基酸合成
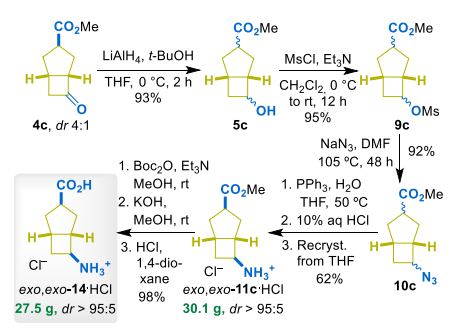
以酮酯4c(dr=4:1)为起始:
● 路线1:还原→甲磺酰化→叠氮化→还原,经THF重结晶得到exo,exo-11c·HCl,再经Boc保护、碱性水解、脱保护得到氨基酸exo,exo-14c
● 路线2:还原胺化(Bn₂NH/NaBH (OAc)₃)→氢解脱苄→重结晶得到exo,endo-11c·HCl,同理得到氨基酸exo,endo-14c
3.5 单晶XRD与出口矢量图(EVP)表征
通过单晶XRD确证两种氨基酸衍生物的相对构型:
● exo,exo-11c·HCl(CCDC:2503937)
● exo,endo-14·TsOH(CCDC:2503938)
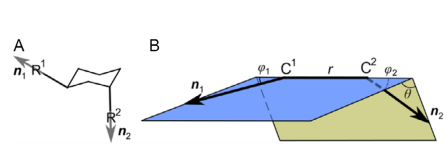
采用出口矢量图(EVP)分析官能团取向:定义两个矢量n₁、n₂,以取代基连接原子为起点,沿键方向延伸;用r、φ₁、φ₂、θ四个几何参数描述相对取向,用于骨架对比分析。
关键结论
● exo,exo-构型:
o 矢量呈近似线性(轻微扭曲)
o 几何特征与1,4-二取代苯高度吻合
→ 可作为苯环对位电子等排体
● exo,endo-构型:
o 呈T型/正交几何
o 单环骨架中极为少见
→ 提供独特官能团正交排布,拓展药物分子设计空间
4、结论
本工作建立了一套简洁、可放大、非对映选择性的路线,用于制备非对映纯3,6-二取代双环[3.2.0]庚烷。
● 核心:烯酮[2+2]环加成(确立C-1、C-3、C-5相对构型)+立体选择性还原/还原胺化(确立C-6手性)
●规模:可制备27.5克(exo,exo)、26.7克(exo,endo)级别的纯非对映体砌块
● 产物:涵盖双环氨基酸、氨基醇等药物导向砌块
● 结构价值:
o exo,exo-骨架:可作为1,4-二取代苯的饱和电子等排体
o exo,endo-骨架:呈现罕见T型正交几何
该方法原料易得、操作安全、无需剧毒试剂,适合工业化放大。结合动力学拆分潜力,未来可进一步拓展至手性富集化合物的制备。所得砌块与结构数据可直接应用于合成有机化学与药物早期发现。

