桥环化合物在新药研发中扮演着越来越重要的角色,其独特的结构和性质为解决药物研发中的关键挑战提供了有力工具。以下是它们在新药研发中的主要作用和优势:
1、增强构象刚性和稳定性:
固定活性构象: 桥环结构通过限制分子的自由旋转和折叠,将分子锁定在特定的三维构象(生物活性构象)。这减少了分子在结合靶标蛋白之前需要付出的构象熵代价,显著提高与靶标的结合亲和力(Potency)。
提高代谢稳定性: 刚性结构使得分子不易被代谢酶(如细胞色素P450)识别和降解,延长药物在体内的半衰期,可能降低给药频率和剂量。
减少非特异性结合: 更精确的构象可以减少与非靶标蛋白或生物大分子的非特异性相互作用,提高选择性,从而降低脱靶副作用的风险。
2、改善药代动力学性质:
提高膜通透性: 桥环结构通常能增加分子的脂溶性,这有利于药物穿透细胞膜(如血脑屏障BBB),到达胞内靶点或中枢神经系统靶点。
优化溶解度: 虽然刚性可能降低水溶性,但通过合理的分子设计(如引入极性基团或在特定位置修饰),可以在保持刚性的同时平衡脂溶性和水溶性,改善口服吸收和生物利用度。
降低清除率: 如前所述,代谢稳定性的提高直接导致清除率降低。
3、提供独特的三维空间和立体化学特征:
探索新的化学空间: 桥环结构创造了许多天然产物中常见的、但在传统平面或单环结构中难以实现的独特三维形状和立体化学环境。这有助于药物化学家探索更广阔的化学空间,寻找与复杂生物靶点(如蛋白-蛋白相互作用界面、别构位点)更契合的新型分子。
增强靶标选择性: 独特的形状可以更精确地匹配特定靶标蛋白的活性口袋,提高对相关同源蛋白(如激酶亚型、受体亚型)的选择性,减少脱靶效应。
4、突破“类药五规则”限制:
传统的“类药五规则”强调分子量≤500、氢键供体≤5、氢键受体≤10、脂水分配系数logP≤5、可旋转键≤10等。许多复杂的生物靶点(如PPI靶点)需要更大、更刚性的分子来有效结合。
桥环化合物通过减少可旋转键的数量(通常非常少),可以在分子量相对较大时仍然保持较好的类药性(如良好的口服生物利用度、代谢稳定性)。它们能够突破传统规则的束缚,成为靶向“难成药”靶点的重要武器。
5、提高配体效率:
配体效率衡量单位分子量或非氢原子对结合能的贡献。由于桥环结构能显著提高结合亲和力(ΔG)而分子量增加相对可控(尤其是与增加大量可旋转键相比),它们通常能提供更高的配体效率,意味着用更小的结构变化获得更大的效力提升。
6、作为优势骨架和分子工具:
优势骨架: 一些桥环体系(如金刚烷、降冰片烷、双环[1.1.1]戊烷、立方烷及其衍生物)因其卓越的性质(刚性、稳定性、可修饰性、独特的空间填充特性)而被视为“优势骨架”,被广泛应用于苗头化合物优化和骨架跃迁中。
生物电子等排体: 桥环片段(如双环[1.1.1]戊烷-1-基)常被用作叔丁基、苯环、炔基等的空间受限生物电子等排体,用以改善溶解度、降低logP、提高代谢稳定性或引入特定的三维特征。
连接基团: 在双功能分子(如PROTACs、分子胶)中,桥环结构可以作为刚性的连接基团,精确控制两个配体(E3连接酶配体和靶蛋白配体)之间的距离和方向,优化三元复合物的形成效率。
近年来,各种各样的新颖桥环化合物不断涌现,层出不穷。在这其中,2-氧二环[2.2.2]辛烷作为苯环对位取代的理想电子等排体,也受到了很多药化人员的关注。从下面报道的数据中可以看出,2-氧二环[2.2.2]辛烷与苯环的参数是最接近的。
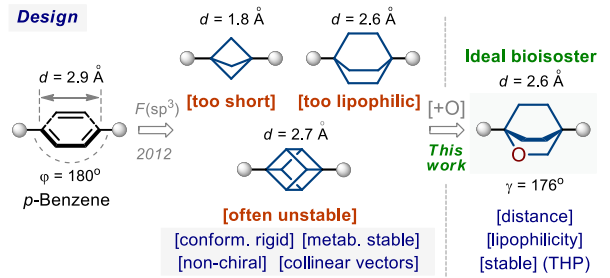
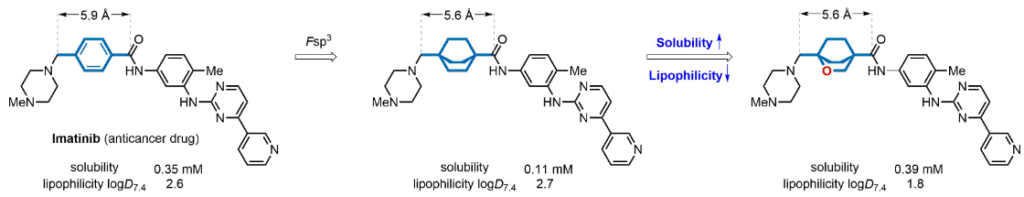
研究人员对药物分子Imatinib进行了结构改造,将苯环区域先后改造成二环[2.2.2]辛烷和2-氧二环[2.2.2]辛烷,从溶解度和LogD来看,2-氧二环[2.2.2]辛烷的溶解度提高了,而亲脂性LogD降低了,相比而言,二环[2.2.2]辛烷的亲脂性太高了。
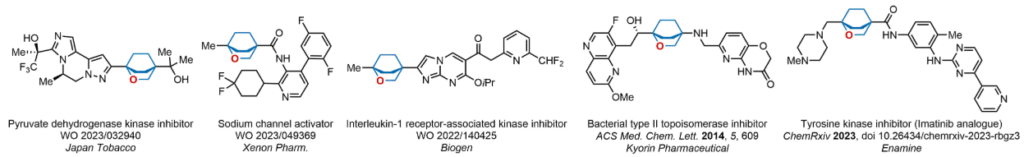
在众多的文献报道中,我们挑选了几个化合物作为示例进行展示。
我们Enamine对2-氧二环[2.2.2]辛烷的合成早有布局,并且发表了文章报道了我们的工作。感兴趣的朋友,可下载该文章进行阅读(ChemRxiv, 2023, 1-11; An “Ideal” Bioisoster of the para-substituted Phenyl Ring)。
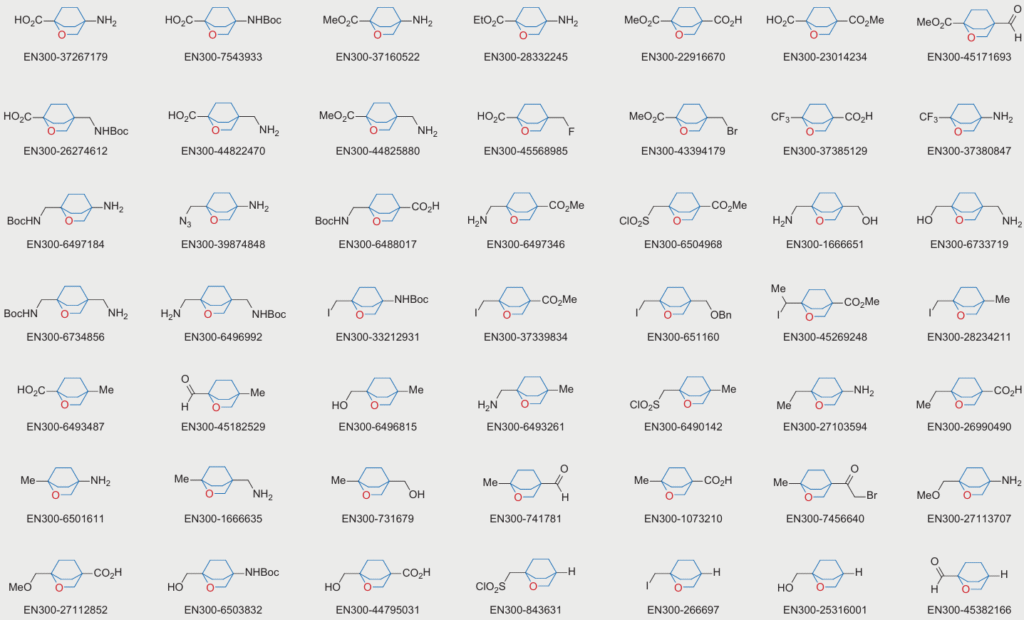
Enamine紧跟药物研究前沿,推出了一系列2-氧二环[2.2.2]辛烷化合物,部分化合物如下。这些化合物有单官能团的羧酸,醛,醇,胺,磺酰氯,碘代物,溴代甲基酮,还有双官能团的分子砌块,可以运用在不同的化学反应和骨架改造上。
更多详情,点击此处。如有需求,欢迎垂询!

