五氟化硫基团(−SF5)因其独特的电子和亲脂性,已成为现代合成化学中越来越有价值的手段。作为−CF3和tBu组的生物电子等排体,它在制药、农用化学品和材料科学应用方面引起了极大的兴趣,特别是在新药开发中,五氟化硫基团(−SF5)是一个新兴的氟化修饰策略,作为一款超级三氟甲基,因其独特的物理化学性质而受到关注,并且占住了一定的IP高地。
最近,美国化学会志在《Chem. Rev.》上报道了一篇综述,题目为“Synthetic Access to Persulfuranyl Scaffolds via Direct and Indirect Methods”(doi/10.1021/acs.chemrev.5c00131),该文章全面概括和总结了五氟化硫的最新进展。以SF5Cl合成开始,通过多种方法学的开发,从多角度去拓宽试剂的应用,包括运用直接和间接方法,如五氟硫基化多米诺环化反应,α-甲基/α-苯基苯乙烯的五氟硫基化反应,光化学反应等,合成了不同的分子砌块,如炔烃,烯烃,羰基,三元环,四元环,稠环,螺环,桥环,在合成化学中充分使用了五氟化硫基团,促进了−SF5有效地结合到不同的分子骨架中。
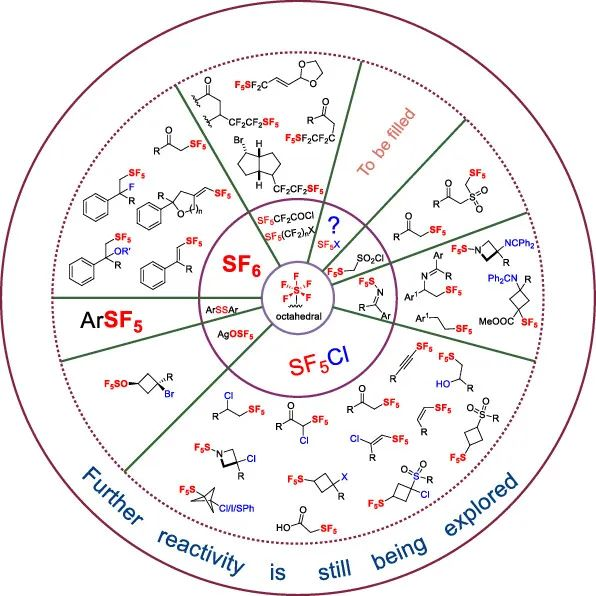
五氟化硫化合物在药物合成领域运用最广,文献报道也最多,该综述不吝笔墨,列举了五氟化硫化合物在不同靶点的应用。
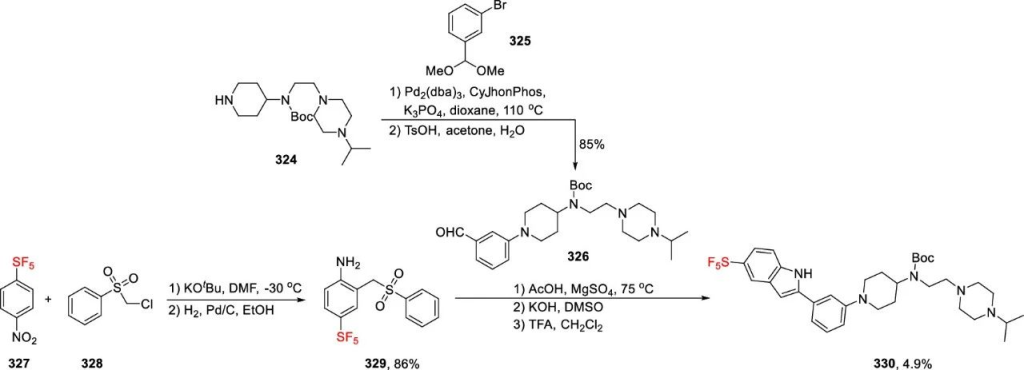
如Huryn与Wipf报道了以4-SF₅-硝基苯(327)为原料合成五氟硫烷基吲哚抑制剂。
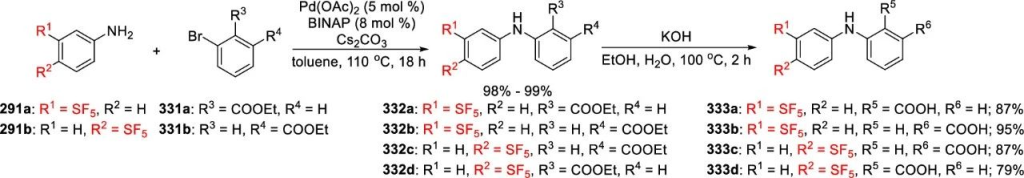
Bolm团队通过将对/间位SF₅取代苯胺291与邻/间位溴代苯甲酸甲酯331结合,合成了四种含SF₅的氟芬那酸类似物333。
Zhang团队以4-SF₅取代苯酚334为起始原料,合成了具有抗肿瘤特性的环氧化酶-2抑制剂苯并吡喃类似物。
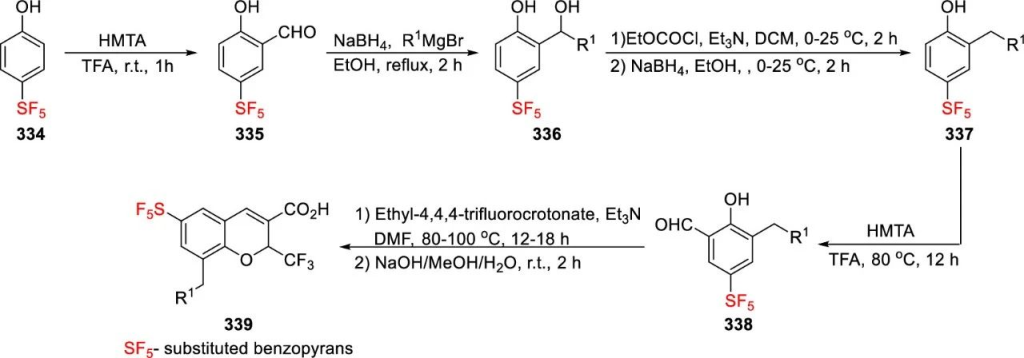
Vincent与Duncton以4-SF₅取代苯甲酸340为原料,报道了TRPV4受体拮抗剂341的合成。
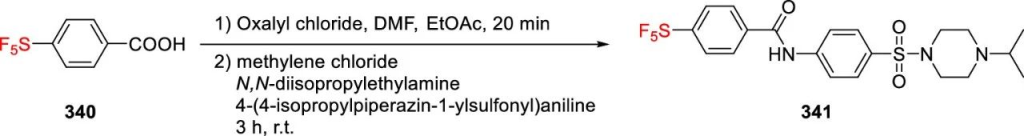
Westwell团队利用SF₅取代苯甲醛合成了含SF₅的鬼臼毒素类似物。将1,10-菲啰啉胺342、四酮酸343与SF₅取代苯甲醛344在乙醇中回流反应,分别以78%和76%的收率获得间位和对位SF₅取代的羟基-4-氮杂鬼臼毒素化合物345。
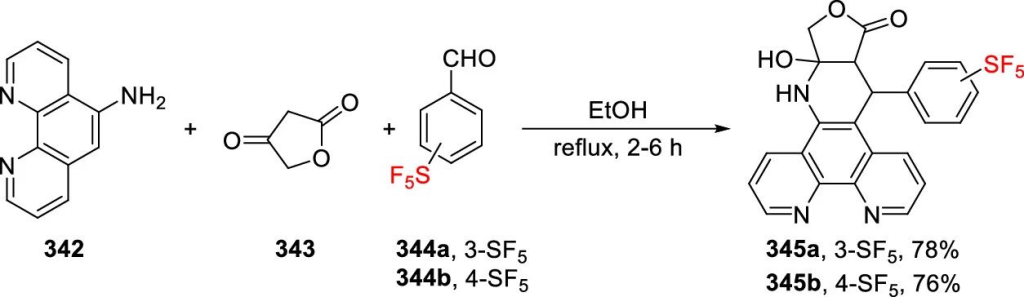
Vazquez团队合成了具有潜在抗菌活性的含SF₅三氯卡班类似物。
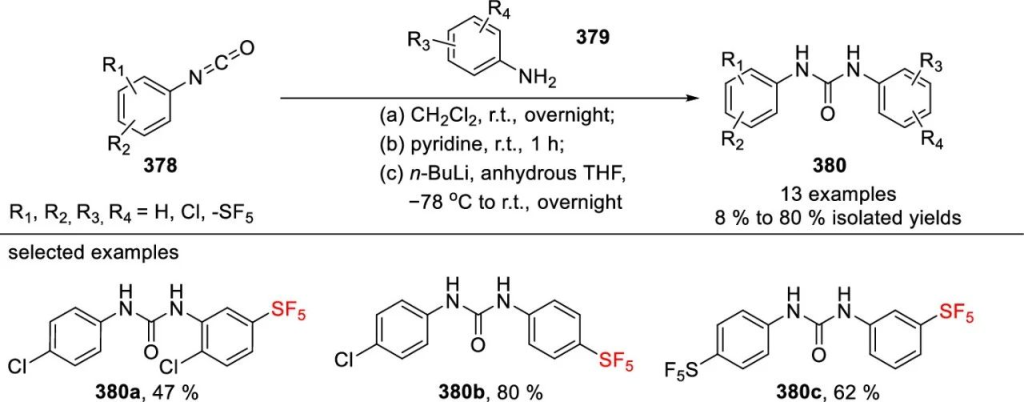
五氟化硫化合物在药物合成领域的运用实例,比比皆是,不一而足,笔者在此也不赘述了。五氟化硫基团作为在新药开发中一种新兴的策略,它的特点总结如下:
1. 增强药物代谢稳定性
- 抗代谢降解:SF₅基团的高稳定性(C-S键能高、空间位阻大)可减少药物被细胞色素P450酶代谢的速度,延长半衰期。
- 案例:在抗炎或抗肿瘤化合物中引入SF₅,可降低羟基化或氧化代谢的发生率。如此综述中提到的, N-SF5化合物在多种介质(胎牛血清、磷酸盐缓冲液、柠檬酸盐缓冲液、pH2盐酸、DMSO、乙腈、甲醇)中均表现卓越稳定性(24小时无分解)。
2. 调节脂溶性与渗透性
- 高亲脂性:SF₅的LogP值显著高于-CF₃,可能改善药物穿过细胞膜的能力,尤其对中枢神经系统(CNS)药物设计有价值。N-SF5修饰的脾酪氨酸激酶(SYK)抑制剂展现出显著增强的亲脂性(log D7.4>5,N-SO2Me类似物仅2.1)。
- 平衡设计:需注意过度亲脂性可能降低水溶性,需通过分子其他部分(如引入极性基团)优化药代动力学。
3. 生物电子等排效应
- 替代传统基团:SF₅可作为-CF₃、-OCF₃或叔丁基的电子等排体,提供类似的立体效应但不同的电子特性,可能增强靶标结合力。N-SF5可作为磺胺类生物电子等排体。
- 案例研究:某些激酶抑制剂中,SF₅替换后显示更高的选择性或亲和力。
4. 提高靶标结合特异性
- 立体效应:SF₅的八面体几何结构可能填补靶蛋白疏水口袋的特殊空间,减少脱靶效应。
- 静电作用:部分研究表明,SF₅的极化特性可能参与弱氢键或偶极相互作用。
五氟化硫化合物在专利中也多有报道,实例如下:
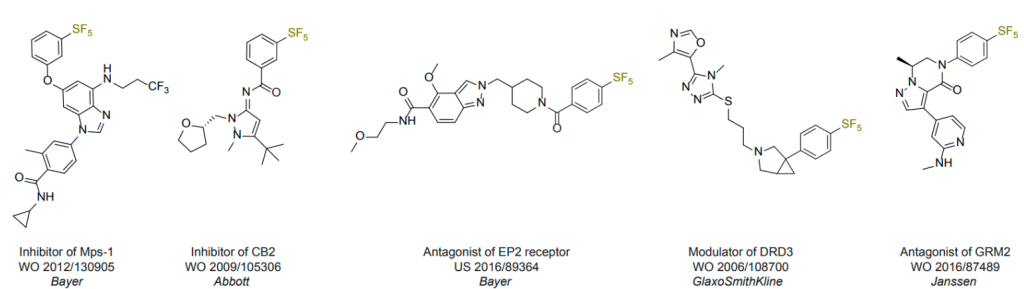
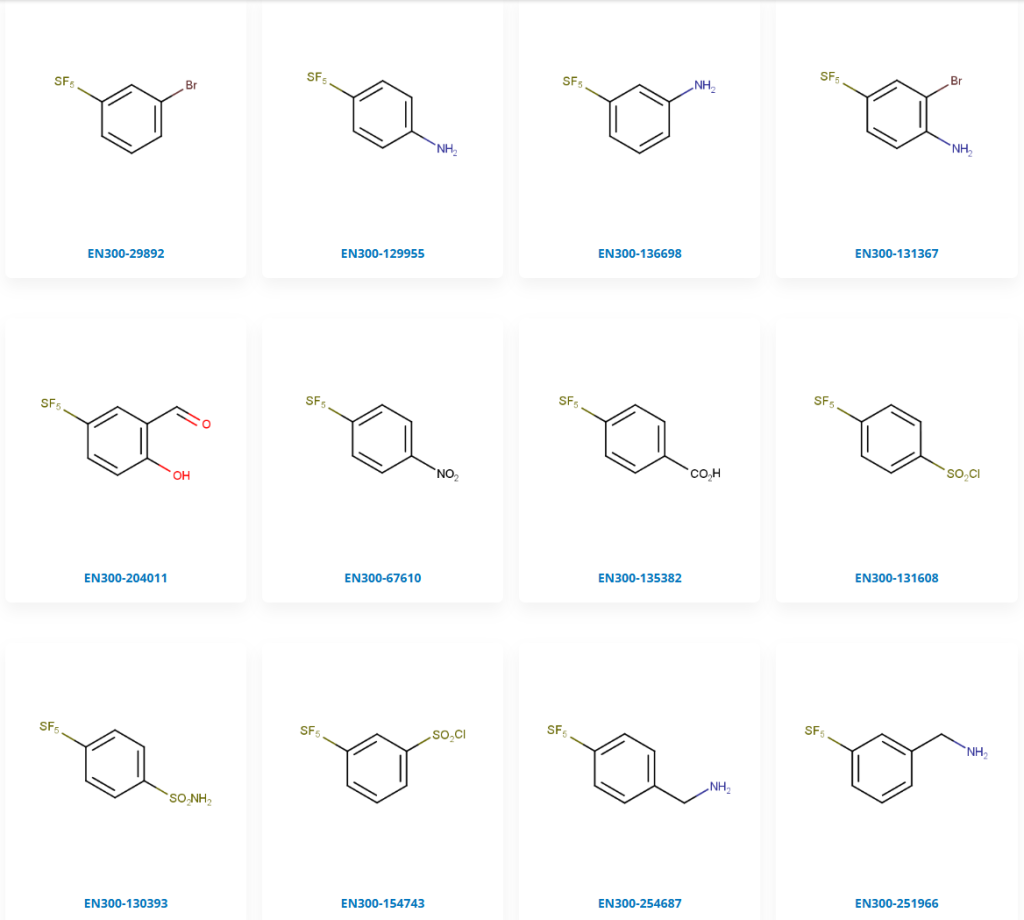
Enamine紧跟药物研究前沿,推出了一系列SF₅化合物,部分化合物如下。这些化合物可以运用在不同的化学反应上,如Suzuki反应,Buchwald反应,酰胺化反应,磺酰胺化反应,还原胺化反应,总有一款适合您。